
| A. | 改用浓硫酸 | B. | 加热 | ||
| C. | 加入少量CuSO4固体 | D. | 将铁块改成铁粉 |
分析 该反应中,Fe过量,生成氢气由硫酸决定,增大反应物浓度、升高温度、增大反应物接触面积或形成原电池反应,不影响生成氢气的总量,都能增大反应速率,据此分析解答.
解答 解:A.改用浓硫酸,浓硫酸与铁发生钝化,反应立即停止,所以不能加快反应速率,故A错误;
B.加热,增大活化分子百分数,所以反应速率加快,生成氢气总量不变,故B正确;
C.加入少量CuSO4固体,铁置换出Cu,形成原电池反应,反应速率增大,由于铁过量,则生成氢气的总量不受影响,故C正确;
D.将铁块改成铁粉,增大反应物接触面积,反应速率加快,生成氢气总量不变,故D正确;
故选A.
点评 本题考查反应速率影响因素,明确化学反应速率影响原理即可解答,浓度、温度、催化剂、压强等可能都影响反应速率,注意:浓硫酸与铁发生钝化,题目难度不大.


 开心练习课课练与单元检测系列答案
开心练习课课练与单元检测系列答案科目:高中化学 来源: 题型:选择题
| A. | 0.15 mol/L的盐酸 | B. | 0.10mol/L的硫酸 | ||
| C. | 0.15 mol/L的醋酸 | D. | 0.10mol/L的氢硫酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 实验操作 | 现象 | 结论 |
| A | 等体积pH=2的HX和HY两种酸分别与足量的铁反应,用排水法收集气体 | HX放出的氢气多且反应速率快 | HX酸性比HY强 |
| B | 向某溶液中滴入氯化钡溶液和稀硝酸 | 生成白色沉淀 | 说明原溶液含Ba2+ |
| C | 在稀硫酸中加入铜,再加入硝酸钠固体 | 开始无现象,后铜逐步溶解,溶液变蓝,有气泡产生 | 硝酸钠可以加快铜与稀硫酸的反应速率 |
| D | 将一铝箔放在酒精灯外焰上灼烧 | 铝箔熔化但不滴落 | 铝箔表面生成致密的Al2O3薄膜,且Al2O3熔点高于Al |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
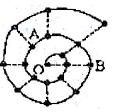 某同学在研究前18号元素时发现,可以将它们排成如图所示的“蜗牛”形状,图中每个“•”代表一种元素,其中O点代表氢元素.下列说法中错误的是( )
某同学在研究前18号元素时发现,可以将它们排成如图所示的“蜗牛”形状,图中每个“•”代表一种元素,其中O点代表氢元素.下列说法中错误的是( )| A. | A、B组成的化合物中不可能含有共价键 | |
| B. | 虚线相连的元素处于同一族 | |
| C. | B元素是图中金属性最强的元素 | |
| D. | 离O点越远的元素原子半径越大 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 二氧化硫能使高锰酸钾酸性溶液迅速褪色 | |
| B. | 可以用澄清石灰水鉴别二氧化硫和二氧化碳 | |
| C. | 硫粉在过量的纯氧中燃烧可以生成三氧化硫 | |
| D. | 少量二氧化硫通入浓的氯化钙溶液中能生成白色沉淀 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 将SO2通入Fe3+溶液中:2Fe3++SO2+2H2O═2Fe2++SO42-+4H+ | |
| B. | NaClO溶液与FeCl2溶液混合:Fe2++2ClO-+2H2O═Fe(OH)2↓+2HClO | |
| C. | 将氯化亚铁溶液和稀硝酸混合:Fe2++4H++NO3-═Fe3++2H2O+NO↑ | |
| D. | 将磁性氧化铁溶于盐酸:Fe3O4+8H+═3Fe3++4H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 电解法精炼铜时,以粗铜作阴极,纯铜作阳极 | |
| B. | 用pH均为2的盐酸和醋酸分别中和等物质的量的NaOH,消耗盐酸的体积大 | |
| C. | 一定温度下,反应2Mg(S)+CO2(g)=2MgO(S)+C(s)能自发进行,则该反应△H<0 | |
| D. | 常温时,0.1mol•L-l CHCOOH 溶液加水稀释,$\frac{c(C{H}_{3}CO{O}^{-})}{c(C{H}_{3}COOH)•c(O{H}^{-})}$的值不变 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2-丙醇 | B. | 2-丁醇 | C. | 1-戊醇 | D. | 2-甲基-2-丙醇 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 为了给人类一个美好蓝天,化工企业推进脱硫、脱硝、除尘等设施改造,能大量减排SO2、NO2 | |
| B. | “PM2.5”是指大气中直径小于或等于2.5×10-6m的细小颗粒物,这些颗粒扩散在空气中形成胶体 | |
| C. | 实验场所严禁携带食物;禁止用饮料瓶装化学药品,防止误食 | |
| D. | 西非国家爆发的埃博拉疫情呈加速蔓延之势,已知该病毒对化学药品敏感,双氧水、“84”消毒液均可以将病毒氧化而达到消毒的目的 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com