
19g某二价金属的氯化物ACl2中含有0.4mol Cl﹣离子,ACl2的摩尔质量是95g/mol,相对分子质量是95,A的相对原子质量是24.
 口算能手系列答案
口算能手系列答案科目:高中化学 来源: 题型:
下列说法不正确的是()
A. 某有机物燃烧只生成CO2和H2O,且二者物质的量相等,则此有机物的组成为CnH2n
B. 一种烃在足量的氧气中燃烧并通过浓硫酸,减少的总体积就是生成的水蒸气的体积
C. 某气态烃CxHy与足量O2恰好完全反应(温度>100℃),如果反应前后气体体积不变,则y=4
D. 相同质量的烃,完全燃烧,消耗O2越多,烃中含H量越高
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关化学反应速率的说法正确的是()
A. 用铁片和稀硫酸反应制取氢气时,改用98%的浓硫酸可以加快产生氢气的速率
B. 100mL2mol•L﹣1的盐酸跟锌片反应,加入适量的氯化钠溶液,反应速率不变
C. SO2的催化氧化是一个放热的反应,所以升高温度,反应速率减慢
D. 汽车尾气中的NO和CO可以缓慢反应生成N2和CO2,减小压强反应速率减慢
查看答案和解析>>
科目:高中化学 来源: 题型:
0.5L 1mol/L FeCl3溶液中的Cl﹣的物质的量浓度为()
A. 3 mol/L B. 1.5 mol/L C. 1 mol/L D. 0.5 mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
100mL 0.3mol/L Na2SO4溶液和50mL 0.2mol/L Al2(SO4)3溶液混合后,溶液中SO42﹣的物质的量浓度约为()
A. 0.20mol/L B. 0.25mol/L C. 0.4mol/L D. 0.5mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
取1.43g Na2CO3•10H2O溶于水配成100mL溶液,求:
(1)Na2CO3溶液的物质的量浓度
(2)Na+物质的量浓度
(3)取出20ml该溶液用水稀释,使Na2CO3溶液的物质的量浓度变为0.004mol/L,求加入水的体积(设稀释时,对溶液体积的影响忽略不计)
查看答案和解析>>
科目:高中化学 来源: 题型:
VL Fe2(SO4)3溶液中含有Fe3+mg,则溶液中SO42﹣的物质的量浓度为()
A. 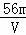 mol/L B.
mol/L B. 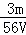 mol/L C.
mol/L C. 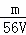 mol/L D.
mol/L D. 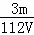 mol/L
mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
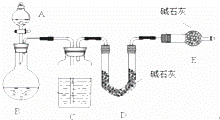
某化学兴趣小组采用下列方法测定Na2SO3样品中Na2SO4的质量分数.
【方法一】测 SO2质量法采用如图所示装置,通过实验测定生成SO2的质量.
(1)C中盛放的试剂是 ,E装置的作用是
(2)若实验前称取m1g样品,再测得SO2的质量为m2g,则可得Na2SO4质量分数,其中m2是通过测定 (填装置符号)装置在实验前后的质量差得到的.该方法的缺点是(只答一点).
【方法二】测沉淀质量法
第一步:称取m3g样品,置于小烧杯中 第二步:向小烧杯中加入足量稀盐酸,加热
第三步:再向小烧杯中加入足量BaCl2溶液,然后过滤、洗涤 第四步:干燥沉淀,称重为m4g
(3)简述洗涤沉淀的方法: .
(4)若m3=2m4 则试样中Na2SO4的质量分数为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
对下列化学反应的热现象,不正确的说法是()
A. 有些放热反应发生时需要加热
B. 化学反应一定既有物质变化又有能量变化
C. 吸热反应都需要加热后才能发生
D. 化学反应热效应数值与反应物质多少有关
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com