
| A. | 9g超重水(3H216O)含中子数为6NA | |
| B. | 标准状况下,22.4LCCl4含有的分子数目为NA | |
| C. | 常温常压下,16g甲烷含有共价键数目为4NA | |
| D. | 1L0.1mol•L-1的NaHCO3溶液中HCO3-和CO32-离子数之和为0.1NA |
分析 A.求出超重水的物质的量,然后根据1mol超重水中含12mol中子;
B.气体摩尔体积使用对象为气体;
C.质量转化为物质的量,结合1个甲烷分子含有4个C-H键;
D.碳酸氢钠溶液中,碳酸氢根离子部分水解生成碳酸和氢氧根离子,部分电离生成碳酸根离子和氢离子,部分以碳酸氢根离子存在.
解答 解:A.9g超重水的物质的量为n=$\frac{9g}{22g/mol}$=$\frac{9}{22}$mol,而1mol超重水中含12mol中子,故$\frac{9}{22}$mol超重水中含4.9mol中子即4.9NA个,故A错误;
B.标况下四氯化碳为液体,不能使用气体摩尔体积,故B错误;
C.常温常压下,16g甲烷物质的量为$\frac{16g}{16g/mol}$=1mol,有共价键数目为1mol×4×NA=4NA,故C正确;
D.碳酸氢钠溶液中,碳酸氢根离子部分水解生成碳酸和氢氧根离子,部分电离生成碳酸根离子和氢离子,部分以碳酸氢根离子存在,依据碳原子个数守恒:1L0.1mol•L-1的H2CO3、NaHCO3溶液中HCO3-和CO32-离子数之和为0.1NA,故D错误;
故选:C.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,注意盐类水解、电离的实质,题目难度不大.


 轻松课堂单元测试AB卷系列答案
轻松课堂单元测试AB卷系列答案 小题狂做系列答案
小题狂做系列答案科目:高中化学 来源: 题型:选择题
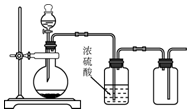
| A. | 用锌和稀硫酸制备H2 | B. | 用铜和稀硝酸制备NO | ||
| C. | 用30%H2O2水溶液和MnO2制备O2 | D. | 用MnO2和浓盐酸制备Cl2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 实验 | 现象 | 结论或解释 |
| A | 纯净的H2在Cl2中燃烧 | 安静地燃烧,并发出苍白色火焰 | 说明燃烧不一定需要氧气参加 |
| B | 分别将蘸有浓氨水和浓硫酸的玻璃棒靠近 | 产生白烟 | NH3能和酸反应生成了相应的铵盐 |
| C | 把SO2通入高锰酸钾溶液中 | 酸性高锰酸钾溶液褪色 | 说明SO2只具有漂白性 |
| D | 高温下,SiO2与纯碱混合加热,产生气体通入澄清石灰水 | 石灰水变浑浊 | 说明硅酸的酸性比碳酸强 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 析氢腐蚀 | B. | 吸氧腐蚀 | C. | 化学腐蚀 | D. | 置换反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 实验操作 | 实验现象 | 结论 |
| A | 将少量Fe(NO3)2试样加水溶解后,滴加稀硫酸酸化,再滴加KSCN溶液 | 溶液变成血红色 | Fe(NO3)2试样已变质 |
| B | 向甲苯中滴加少量酸性高锰酸钾溶液 | 高锰酸钾溶液褪色 | 甲苯发生了氧化反应 |
| C | 常温下分别测定浓度均为0.1mol/L的Na2SiO3溶液和Na2CO3溶液的pH | pH:Na2SiO3>Na2CO3 | 非金属性:Si>C |
| D | 将少量某无色气体通入澄清石灰水中 | 出现白色沉淀 | 该气体一定是CO2 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源:2017届四川省高三上10月月考化学试卷(解析版) 题型:填空题
物质的化学变化乍看起来,好像十分复杂,难以把握,而实际上是有规律可循的。认识化学原理并将化学原理应用于实际正是化学的魅力所在。
I.在恒容密闭容器中通入X并发生反应:2X(g) Y(g),温度T1、T2下X的物质的量浓度c(x)随时间t变化的曲线如图所示
Y(g),温度T1、T2下X的物质的量浓度c(x)随时间t变化的曲线如图所示
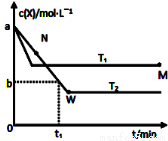
①该反应的化学平衡常数表达式为:_____________
②M点的正反应速率v正_________(填“>”、“=”或“<”)N点的逆反应速率v逆;T2下,在0~t1时间内,v(Y)=_______________;该反应进行到M点放出的热量_________(填“>”、“=”或“<”)进行到W点放出的热量。
③M点时再加入一定量的X,平衡后X的转化率___________(填“增大”、“减小”或“不变”)
II.0.1mol/LNaHCO3溶液与0.1mol/L NaOH溶液等体积混合,所得溶液中离子浓度由大到小的顺序为_________________
III.下图是某种燃料电池原理示意图:
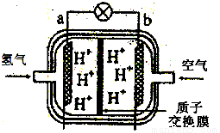
(1)该燃料电池工作过程中,其正极反应式为:________________________。
(2)若用此燃料电池作为电源向铁制品上镀上一层铜,则铁制品要连接在燃料电池的__________极(填“a”或“b”)上.若用此燃料电池电解精炼银,应使粗银作电解池的____________极,使用AgNO3和HNO3的混合溶液作电解液,若阴极有少量红棕色气体生成,则生成该气体的电极反应式为:__________________。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年江西省高二上第一次月考化学试卷(解析版) 题型:选择题
少量铁粉与100mL0.01mol/L的稀盐酸反应,反应速率太慢。为了加快此反应速率而不改变H2的产量,可以使用如下方法中的( )
①加H2O ②加NaOH固体 ③滴入几滴浓盐酸 ④加CH3COONa固体⑤加NaCl溶液 ⑥滴入几滴硫酸铜溶液 ⑦升高温度(不考虑盐酸挥发) ⑧改用10mL0.1mol/L盐酸.
A.①⑥⑦ B.③⑤⑧ C.③⑦⑧ D.⑤⑦⑧
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com