
W、X、Y、Z是周期表前36号元素中的四种常见元素,其原子序数依次增大。W、Y的氧化物是导致酸雨的主要物质,X的基态原子核外有7个原子轨道填充了电子且有1个轨道上只有1个电子,Z能形成砖红色的Z2O和黑色的ZO两种氧化物。
(1)W位于元素周期表第________周期第________族。W的气态氢化物稳定性比
H2O(g)________(填“强”或“弱”)。
(2)Y的基态原子核外电子排布式是______________,Y的第一电离能比X的________(填“大”或“小”)。
(3)Y的最高价氧化物对应水化物的浓溶液与Z的单质反应的化学方程式是_______。
(1)2 ⅤA 弱 (2)1s22s22p63s23p4 大
(3)Cu+2H2SO4(浓)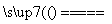 CuSO4+SO2↑+2H2O
CuSO4+SO2↑+2H2O
解析 首先注意题目信息中的“前36号”、“常见元素”、“原子序数依次增大”。W、Y的氧化物是导致酸雨的主要物质,应该是NO2和SO2,再依据“原子序数依次增大”的信息,可知W为N元素,Y为S元素。X的基态原子核外有7个原子轨道填充了电子且有1个轨道上只有1个电子,其核外电子排布式应为1s22s22p63s23p1,该元素应为Al。Z能形成砖红色的Z2O和黑色的ZO两种氧化物,可知Z为Cu。
(1)W(N)位于元素周期表第2周期第ⅤA族。W的气态氢化物为NH3,因N的非金属性比O弱,故NH3稳定性比H2O弱。
(2)Y的基态原子核外电子排布式是1s22s22p63s23p4;Y(S)的原子半径小于X(Al),所以Y(S)对外层电子的吸引力强于X(Al),故Y的第一电离能比X的大。
(3)Y的最高价氧化物对应水化物为H2SO4,其浓溶液(即浓硫酸)与Z的单质(Cu)反应的化学方程式是Cu+2H2SO4(浓)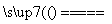 CuSO4+SO2↑+2H2O。
CuSO4+SO2↑+2H2O。


 黎明文化寒假作业系列答案
黎明文化寒假作业系列答案科目:高中化学 来源: 题型:
元素周期表可以划分为5个区,下列有关说法正确的是( )
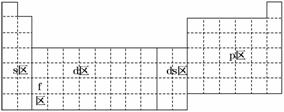
A.s区全部是金属元素
B.p区全部是非金属元素
C.d区内元素原子的价电子排布必为(n-1)d1~10ns2
D.除ds区外,以最后填入电子的轨道能级符号作为区的符号
查看答案和解析>>
科目:高中化学 来源: 题型:
在两支分别盛有Al(OH)3的试管中,向其中一支中滴加足量盐酸,观察到的现象是____________________________,发生反应的离子方程式为__________________________;
向另一支滴加足量NaOH溶液,观察到的现象是________________________,发生反应的
离子方程式为____________________________。由此说明Al(OH)3是一种________氢氧化物。
查看答案和解析>>
科目:高中化学 来源: 题型:
沉淀的生成、溶解和转化在无机物制备和提纯以及科研等领域有广泛应用。已知25℃时,Ksp(BaSO4)=1×10-10,Ksp(BaCO3)=1×10-9。
(1)将浓度均为0.1 mol·L-1的BaCl2溶液与Na2SO4溶液等体积混合,充分搅拌后过滤,滤液中c(Ba2+)=________mol·L-1。
(2)医学上进行消化系统的X射线透视时,常使用BaSO4作内服造影剂。胃酸酸性很强(pH约为1),但服用大量BaSO4仍然是安全的,BaSO4不溶于酸的原因是__________________________________________________。
(用沉淀溶解平衡原理解释)。万一误服了少量BaCO3,应尽快用大量0.5 mol·L-1Na2SO4溶液给患者洗胃,如果忽略洗胃过程中Na2SO4溶液浓度的变化,残留在胃液中的Ba2+浓度仅为________mol·L-1。
(3)长期使用的锅炉需要定期除水垢,否则会降低燃料的利用率。水垢中含有的CaSO4,可先用Na2CO3溶液处理,使之转化为疏松、易溶于酸的CaCO3,而后用酸除去。
①CaSO4转化为CaCO3的离子方程式为:
__________________________________________________;
②请分析CaSO4转化为CaCO3的原理:_________________________________________
__________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法不正确的是( )
A.第一电离能、电负性的周期性递变规律是原子核外电子排布周期性变化的结果
B.电负性的大小也可以作为判断金属性和非金属性强弱的尺度
C.电负性是相对的,所以没有单位
D.分析元素的电负性数值可以看出,金属元素的电负性较大,非金属元素的电负性较小
查看答案和解析>>
科目:高中化学 来源: 题型:
2008年世界环境日,中国提出的主题为“绿色奥运与环境友好型社会”。爱护环境,呵护地球是我们每一个人不可推卸的责任。下列大气污染现象与污染源对应不正确的是( )
A.酸雨——硫的氧化物、氮的氧化物
B.光化学烟雾——碳氢化合物、氮的氧化物
C.臭氧空洞——氟氯烃(即氟利昂) D.温室效应——SO2
查看答案和解析>>
科目:高中化学 来源: 题型:
下图装置是实验室里常见的气体发生装置,用该装置制取、提纯并收集表中的四种气体(a、b、c表示相应仪器中加入的试剂),其中可行的是 ( )
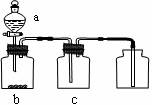 |
气体 | a | b | c | |
| A | NO2 | 浓硝酸 | 铜片 | NaOH溶液 |
| B | SO2 | 浓硫酸 | K2SO3粉末 | 浓硫酸 |
| C | NH3 | 浓氨水 | 生石灰 | 碱石灰 |
| D | CO2 | 稀硫酸 | CaCO3粉末 | NaOH溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
)有A、B、C、D、E五种短周期元素,它们的核电荷数按C、A、B、D、E的顺序增大。C、D都能分别与A按原子个数比为1∶1或2∶1形成化合物;CB可与EA2反应生成C2A和气态物质EB4;E的M层电子数是K层电子数的2倍。
(1)写出下列元素的名称:A______,B______,E______。
(2)画出E的原子结构示意图______。
(3)比较EA2与EB4的熔点高低(填化学式)______>______。
(4)A的氢化物的沸点与同族下一周期元素的氢化物相比,A的氢化物的沸点______(填“高”或“低”),原因是______________________________。
(5) 写出电子式D2A2______,EB4______。
查看答案和解析>>
科目:高中化学 来源: 题型:
已知聚乳酸 可在乳酸菌作用下分解,下列有关聚乳酸的说法正确的是( )
可在乳酸菌作用下分解,下列有关聚乳酸的说法正确的是( )
A.聚乳酸是一种纯净物
B.聚乳酸的单体是
C.聚乳酸是由单体之间通过加聚而合成的
D.聚乳酸是一种酸性高分子材料
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com