
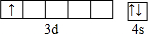
 �����̬ԭ�Ӻ�������Ų�ʽΪ��1s22s22p63s23p63d14s2��ԭ������Ϊ21�����ڵ������ڢ�B�壬���ڽ���Ԫ�أ��γɽ������壬
�����̬ԭ�Ӻ�������Ų�ʽΪ��1s22s22p63s23p63d14s2��ԭ������Ϊ21�����ڵ������ڢ�B�壬���ڽ���Ԫ�أ��γɽ������壬 ��1s22s22p63s23p63d14s2��21��������������
��1s22s22p63s23p63d14s2��21��������������| 5-1��3 |
| 2 |



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A������е�1mol?L-1 NaOH��Һ�еμ�FeCl3������Һ�Ʊ�Fe��OH��3���� |
| B����������ͭ��ĩ������� |
| C����ȡ19.0g SnCl2����100mL����ˮ������1.0mol?L-1 SnCl2��Һ |
| D�������������м��뱥��Na2CO3��Һ������Һ�����ȥ���������е��������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��1mol��������������Ӧ����Na2O��Na2O2ʱ��ʧ������Ŀ��ΪNA |
| B��1mol Na2O2������CO2��Ӧʱ��ת��2NA������ |
| C��1mol/L��NaOH��Һ�к�Na+��ĿNA |
| D��1mol Na2O2�����к��е���������ĿΪ2NA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A������ | B����ϩ | C������ | D���Ȼ��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| 5 |
| 4 |
| 1 |
| 4 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| 1 |
| 2 |
| 1 |
| 2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 �ҹ����ٺ����ʡ�ݣ��ܹ�������ú�ˮ�Ƶö��ֻ�����Ʒ����ͼ���Ժ�ˮ�����ǣ���Ҫ�ɷ�CaCO3����Ϊԭ����ȡ���ֻ�����Ʒ�Ĺ�������ͼ�����й���B�������е�һ�ֱ���Ʒ��E��һ�ֻ��ʣ�N��һ�ֳ����Ľ������ʣ�
�ҹ����ٺ����ʡ�ݣ��ܹ�������ú�ˮ�Ƶö��ֻ�����Ʒ����ͼ���Ժ�ˮ�����ǣ���Ҫ�ɷ�CaCO3����Ϊԭ����ȡ���ֻ�����Ʒ�Ĺ�������ͼ�����й���B�������е�һ�ֱ���Ʒ��E��һ�ֻ��ʣ�N��һ�ֳ����Ľ������ʣ��鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��H++OH-�TH2O��H=-57.3 kJ?mol-1 |
| B��2NaOH��aq��+H2SO4��aq���TNa2SO4��aq��+2H2O��l����H=-114.6 kJ?mol-1 |
| C��2C8H18��l��+25O2��g���T16CO2��g��+18H2O��g����H=-11036 kJ?mol-1 |
| D��2C8H18��l��+25O2��g���T16CO2��g����+18H2O��l����H=-5518kJ?mol-1 |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com