
【题目】下列各溶液中,微粒的物质的量浓度关系正确的是( )
A.![]()
![]() 的
的![]() 溶液中:
溶液中:![]()
B.![]() 的
的![]() 溶液中:
溶液中:![]()
C.![]() 的
的![]() 溶液与
溶液与![]() 的NaOH溶液等体积混合溶液显碱性,其混合溶液中:
的NaOH溶液等体积混合溶液显碱性,其混合溶液中:![]()
D.pH相等的![]() 、
、![]() 、
、![]() 三种溶液中,
三种溶液中,![]() 大小:
大小:![]()
【答案】D
【解析】
![]() 的
的![]() 溶液中,虽然铵根离子水解,但水解是微弱的,所以铵根离子浓度大于硫酸根离子浓度,由于铵根离子水解溶液显酸性,所以
溶液中,虽然铵根离子水解,但水解是微弱的,所以铵根离子浓度大于硫酸根离子浓度,由于铵根离子水解溶液显酸性,所以![]() ,故A错误;
,故A错误;
B.![]() 的
的![]() 溶液中存在质子守恒,水电离出的所有氢氧根离子浓度等于氢离子存在形式浓度总和,
溶液中存在质子守恒,水电离出的所有氢氧根离子浓度等于氢离子存在形式浓度总和,![]() ,故B错误;
,故B错误;
C.![]() 的
的![]() 溶液与
溶液与![]() 的NaOH溶液等体积混合得到等浓度的氯化铵、一水合氨和氯化钠溶液,溶液显碱性说明一水合氨电离程度大于铵根离子水解程度,
的NaOH溶液等体积混合得到等浓度的氯化铵、一水合氨和氯化钠溶液,溶液显碱性说明一水合氨电离程度大于铵根离子水解程度,![]() ,故C错误;
,故C错误;
D.相同pH的![]() 与
与![]() 溶液,都是强酸弱碱盐溶液,溶液显酸性的原因都是铵根离子的水解,而且硫酸根离子和氯离子对铵根离子的水解无影响,因此二者溶液中
溶液,都是强酸弱碱盐溶液,溶液显酸性的原因都是铵根离子的水解,而且硫酸根离子和氯离子对铵根离子的水解无影响,因此二者溶液中![]() 浓度相等,由于
浓度相等,由于![]() 电离时产生
电离时产生![]() 使溶液呈酸性,
使溶液呈酸性,![]() 水解产生的氢离子减少,因此
水解产生的氢离子减少,因此![]() 中
中![]() 的浓度小于
的浓度小于![]() ;则三种溶液中
;则三种溶液中![]() 由大到小的顺序为:
由大到小的顺序为:![]() ,故D正确;
,故D正确;
故选D。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】某学习小组探究稀HNO3、浓HNO3与铜的反应。
装置(尾气处理装置略) | 现象 |
| Ⅰ中开始无明显现象,渐有小气泡生成,越来越剧烈,液面上方出现浅红棕色气体,溶液呈蓝色。 |
Ⅱ中反应剧烈,迅速生成大量红棕色气体,溶液呈绿色。 |
(1)试管Ⅰ中Cu与稀HNO3反应的化学方程式是________。
(2)Ⅱ中反应的速率比Ⅰ中的快,原因是________。
(3)针对Ⅱ中溶液呈绿色的原因,提出假设:
假设1:Cu2+的浓度较大所致;
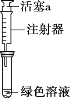
假设2:溶解了生成的NO2。
探究如下:取Ⅱ中绿色溶液,分为两等份。
①取一份于如图所示装置中,_______(填“操作”和“现象”),证实Ⅱ中溶解了NO2。
②向另一份溶液加入_____(填化学试剂),溶液变为蓝色。证实假设1不成立,假设2成立。
(4)对于稀HNO3与铜生成NO、浓HNO3与铜生成NO2的原因,提出两种解释:
解释1.HNO3浓度越稀,溶液中NO3-的数目越少,被还原时,每个NO3-从还原剂处获得较多电子的机会_____(填“增多”或“减少”),因此被还原为更低价态。
解释2.推测下列平衡导致了产物的不同,并通过如下实验证实了推测的合理性。
3NO2+H2O=2HNO3+NO
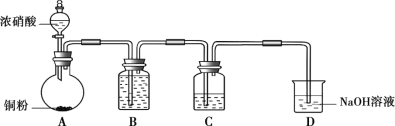
①B中盛放的试剂是________。
②C中盛放Cu(NO3)2和_________。
③该小组证实推测的合理性所依据的实验现象是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、W是原子序数依次增大的短周期主族元素,e、g、h、i、j均是由这些元素组成的二元化合物,i常温常压下为液体,其余均为无色气体。e的摩尔质量为g的2倍,f是元素Z的单质,g物质能使湿润的红色石蕊试纸变蓝,h的组成元素位于同一主族。上述物质的转化关系如图所示。下列说法正确的是

A.原子半径:Y>Z>W>XB.热稳定性:i>g, 沸点:i>e
C.Y与W的含氧酸均是强酸D.h与j均为酸性氧化物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,在一容器内进行某一反应,M、N的物质的量随反应时间变化的曲线如下图所示,则下列叙述中,正确的是( )
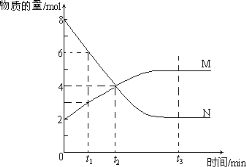
A. 反应的化学方程式一定为2M![]() N
N
B. ![]() 时,逆反应速率一定大于正反应速率
时,逆反应速率一定大于正反应速率
C. ![]() 时,反应达到了化学平衡状态
时,反应达到了化学平衡状态
D. ![]() 时,正反应速率等于逆反应速率
时,正反应速率等于逆反应速率
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用下列实验装置进行相应实验,设计正确且能达到实验目的的是
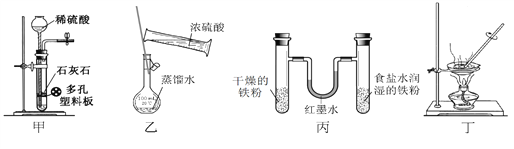
A. 甲用于实验室制取少量CO2 B. 乙用于配制一定物质的量浓度的硫酸
C. 丙用于模拟生铁的电化学腐蚀 D. 丁用于蒸干A1Cl3溶液制备无水AlC13
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下的定容容器中,反应:A(s)+2B(g)![]() C(g) +D(g)。下列不能表明反应
C(g) +D(g)。下列不能表明反应
达到平衡状态的是( )。
A.气体的压强不变B.气体平均相对分子质量不变
C.气体的密度不变D.B物质的量浓度不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碱式氯化铜[CuaClb(OH)cH2O]是一种重要的无机杀虫剂,它可以通过以下步骤制备。步骤1:将铜粉加入稀盐酸中,并持续通空气反应后生成CuCl2。已知Fe3+对该反应有催化作用,其催化原理如图所示
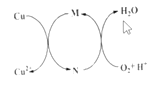
步骤2:在制得的CuCl2溶液中,加入石灰乳充分反应后即可制备碱式氯化铜。下列有关说法正确的是( )
A.a、b、c之间的关系式为:a=b+c
B.图中M、N分别为Fe2+、Fe3+
C.步骤1充分反应后,加入CuO是为了除去Fe3+
D.若制备1molCuCl2,理论上消耗11.2LO2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是可逆反应![]() 在反应过程中的反应速率(v)与时间(t)的关系曲线,下列叙述正确的是( )
在反应过程中的反应速率(v)与时间(t)的关系曲线,下列叙述正确的是( )

A.t1时,反应只向正方向进行B.t2时,反应未达到限度
C.t2~t3,反应已停止D.t2~t3,各物质的浓度不再发生变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下,通过下列反应可实现燃煤烟气中硫的回收:SO2(g)+2CO(g) ![]() 2CO2(g)+S(l) ΔH<0,若反应在恒容的密闭容器中进行,下列说法正确的是( )
2CO2(g)+S(l) ΔH<0,若反应在恒容的密闭容器中进行,下列说法正确的是( )
A.平衡前,随着反应的进行,容器内压强始终不变
B.平衡时,其他条件不变,分离出硫,正反应速率加快
C.平衡时,其他条件不变,升高温度可提高SO2的转化率
D.其他条件不变,使用不同催化剂,该反应的平衡常数不变
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com