
【题目】海水中含有丰富的矿物资源,很多以离子状态存在。今人重视海洋资源的利用,从海洋中获取了多种物质。如图是以海水为原料获取几种物质的流程图:
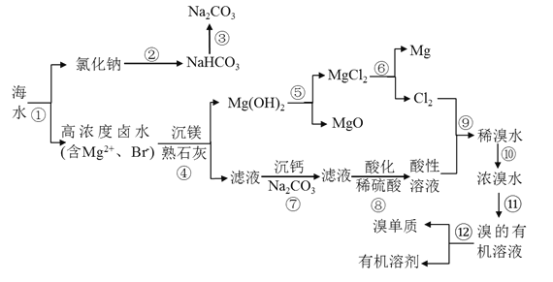
已知Br2在碱性溶液中不能稳定存在。回答下列问题:
(1)步骤②的操作名称为__
(2)步骤②的实现需要向氯化钠溶液中通入CO2、NH3,应先通入_____
(3)步骤⑥的化学方程式为_______步骤⑨的离子方程式为_______
(4)步骤⑧的目的是_____
(5)步骤为萃取分液,需要用到的萃取试剂可以为____(填字母),需要用到的玻璃仪器名称为__
a 裂化汽油 b 苯 c 酒精 d 四氯化碳
【答案】过滤 NH3 MgCl2![]() Mg+Cl2↑ Cl2+2Br-=2C1- + Br2 调节溶液的pH值,使得后续步骤生成的Br2稳定存在 b d 分液漏斗、烧杯
Mg+Cl2↑ Cl2+2Br-=2C1- + Br2 调节溶液的pH值,使得后续步骤生成的Br2稳定存在 b d 分液漏斗、烧杯
【解析】
海水通过蒸发结晶得到氯化钠,氯化钠饱和溶液中通入氨气和二氧化碳气体得到碳酸氢钠晶体,碳酸氢钠灼烧得到碳酸钠;高浓度卤水中加熟石灰氢氧化钙将镁离子转变成氢氧化镁沉淀,氢氧化镁灼烧得到氧化镁,溶于盐酸得到氯化镁,电解熔融的氯化镁得到镁单质和氯气;过滤氢氧化镁后的滤液中加碳酸钠沉淀钙离子,滤液酸化后通氯气得到稀溴水,浓缩后得浓溴水,萃取后得含溴的有机溶液,蒸馏得溴单质,据此分析解答。
(1)由以上分析可知,步骤②是在氯化钠饱和溶液中通入氨气和二氧化碳,充分反应后过滤得到碳酸氢钠,故答案为:过滤;
(2)步骤②的实现需要向氯化钠溶液中通人CO2、NH3,因二氧化碳的溶解度不大,氨气极易溶于水,先通氨气使溶液呈碱性再通二氧化碳有利于二氧化碳的溶解,故答案为:NH3;
(3)步骤⑥是电解熔融的氯化镁得到镁单质,反应为:MgCl2![]() Mg+Cl2↑,步骤⑨是氯气氧化溴离子产生溴单质的过程,反应为:Cl2+2Br-=2C1-+ Br2,故答案为:MgCl2
Mg+Cl2↑,步骤⑨是氯气氧化溴离子产生溴单质的过程,反应为:Cl2+2Br-=2C1-+ Br2,故答案为:MgCl2![]() Mg+Cl2↑;Cl2+2Br-=2C1-+ Br2;
Mg+Cl2↑;Cl2+2Br-=2C1-+ Br2;
(4)步骤⑧加硫酸除去溶液中过量的碳酸钠,使溶液呈酸性,有利于后续产生的溴单质稳定存在,故答案为:调节溶液的pH值,使得后续步骤生成的Br2稳定存在;
(5)a裂化汽油中含有烯烃,能与溴单质反应,不能作为萃取试剂从溴水中萃取溴;c酒精易溶于水,不能作为萃取试剂从溴水中萃取溴;b苯和d四氯化碳均不溶于水,与溴水不反应,且溴单质在两者中的溶解度远大于在水中的溶解度,可以作萃取剂;萃取操作在分液漏斗中进行,萃取后分液还需要用到烧杯,故答案为:bd;分液漏斗、烧杯;


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】合成药物异搏定路线中的某一步骤如下:
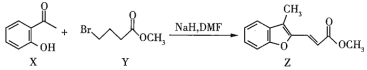
下列说法正确的是( )
A.Z可以发生取代、加成、氧化、加聚反应
B.1molY最多能与1molNaOH发生反应
C.X中所有原子可能在同一平面内
D.1molZ最多能与6molH2发生反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是化学家为纪念元素周期表诞辰150周年而绘制的一种新型元素周期表。在该表中能直观地看出各种元素在地球上的丰度(丰度即该元素占地球所有原子总数的百分比。用该元素所在格子的面积表示丰度的相对大小)。

(1)在图中找到地球上含量最多的元素。其原子结构示意图为___,海水中含量最多的金属离子的结构示意图为___。
(2)宇宙中含量最多的元素为氢元素。氢元素有多种同位素,其中原子核内含有2个中子的核素可表示为___。水分子的电子式为___。
(3)H、C、O和N等丰度较大的元素是构成地球生命物质的主要“材料”。
①H、C、O和N的原子半径从大到小的顺序为___。
②下列与生命活动有关的物质中一定含有H、C、O和N四种元素的是___。
a.蛋白质 b.糖类 c.油脂
(4)Al是地壳中含量最多的金属元素。Al2O3和Al(OH)3均为两性化合物。Al(OH)3和盐酸反应的离子方程式为___,Al(OH)3和NaOH溶液反应的化学方程式为___。试运用元素周期律分析Al2O3和Al(OH)3均为两性化合物的原因是___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,向100mL0.lmol/LNH4Cl溶液中,逐滴滴加0.1mol/LNaOH溶液。NH4+和NH3H2O的变化趋势如图所示(不考虑生成NH3,已知NH3H2O的kb=1.8![]() 10-5),下列说法正确的是( )
10-5),下列说法正确的是( )
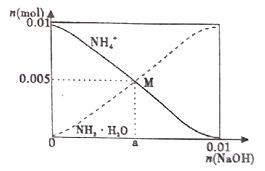
A.a=0.005
B.在M点时,n(H+)—n(OH—)=(0.005—a)mol
C.随着NaOH溶液的滴加,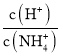 不断增大
不断增大
D.当n((NaOH)) =0.01 mol 时,c ((NH3H2O)![]() c (Na+)
c (Na+)![]() c (OH-)
c (OH-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上制取硫酸铜采用途径I而不采用途径Ⅱ,这样做的优点是

①节省能源 ②不产生污染大气的SO2 ③提高了H2SO4的利用率 ④提高了Cu的利用率
A.仅①②B.仅②③④C.仅①②③D.全部
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】激素类药物己烯雌酚的结构简式如图所示。下列叙述正确的是

A.己烯雌酚是芳香烃
B.1mol己烯雌酚可与6molH2发生加成反应
C.1mol己烯雌酚完全燃烧能生成18molCO2和12 molH2O
D.己烯雌酚苯环上的一氯代物有两种(不包括立体异构)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Q、X、Y和Z为短周期元素,它们在周期表中的位置如图所示,这4种元素的原子最外层电子数之和为22。下列说法正确的是
![]()
A. Y的原子半径比X的大
B. Q的最高价氧化物的水化物的酸性比Z的强
C. X、Y和氢3种元素形成的化合物中都只有共价键
D. Q的单质具有半导体的性质,Q与Z可形成化合物QZ4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A. 氢氧燃料电池放电时化学能全部转化为电能
B. 反应4Fe(s)+3O2(g)![]() 2Fe2O3(s)常温下可自发进行,该反应为吸热反应
2Fe2O3(s)常温下可自发进行,该反应为吸热反应
C. 3 mol H2与1 mol N2混合反应生成NH3,转移电子的数目小于6×6.02×1023
D. 在酶催化淀粉水解反应中,温度越高淀粉水解速率越快
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应的离子方程式书写正确的是( )
A.铁与Fe(NO3)3溶液反应:Fe+2Fe3+=3Fe2+
B.铝与氢氧化钠溶液反应:A1+2OH-=![]() +H2↑
+H2↑
C.Cu(OH)2与稀硝酸反应:Cu(OH)2+2H+=Cu2++2H2O
D.醋酸与Na2CO3溶液反应:2H++![]() =CO2↑+H2O
=CO2↑+H2O
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com