
【题目】请将符合题意的下列变化的序号填在对应的横线上:①碘的升华;②氧气溶于水;③氯化钠溶于水;④烧碱熔化;⑤氯化氢溶于水;⑥氯化铵受热分解。
(1)化学键没有被破坏的是__________;仅发生离子键破坏的是__________;
(2)即发生离子键破坏、又发生共价键破坏的是____________________;
(3)N2的电子式为__________;Na2O2的电子式为___________;CO2的电子式为_________;
(4)用电子式表示MgCl2的形成过程 _____________________;
(5)已知拆开1 mol H—H键、1 mol N≡N、1 mol N—H键分别需要吸收的能量为436 kJ、946 k J、391 k J。则由N2和H2反应生成1 mol NH3 需要放出_____的热量。
【答案】①②③④⑥![]()
![]()
![]()
![]() 46 kJ
46 kJ
【解析】
(1)①碘的升华时,碘由固态转化为气态,只是物质状态发生变化,化学键不被破坏;②氧气溶于水时,氧气分子存在于水中,化学键不被破坏;③氯化钠溶于水时,氯化钠在水分子的作用力电离出钠离子和氯离子,离子键被破坏;④烧碱熔化时,NaOH电离出钠离子和氢氧根离子,离子键被破坏;⑤氯化氢溶于水,氯化氢在水分子的作用下电离出氢离子和氯离子,共价键被破坏;⑥氯化铵受热分解生成氨气和氯化氢,离子键和共价键被破坏。根据以上分析解答(1)(2)两个问题。
(3)N2为共价分子形成氮氮三键;Na2O2为离子化合物,钠离子和过氧根离子间为离子键;CO2为共价化合物,碳氧间形成双键。
(4)氯化镁为离子化合物,镁原子失电子,氯原子得电子。
(5)化学反应中,化学键断裂吸收能量,形成新化学键放出能量,根据方程式计算分别吸收和放出的能量,以此计算反应热并判断吸热还是放热。
(1)①碘的升华时,碘由固态转化为气态,只是物质状态发生变化,化学键不被破坏;
②氧气溶于水时,氧气分子存在于水中,化学键不被破坏;
③氯化钠溶于水时,氯化钠在水分子的作用力电离出钠离子和氯离子,离子键被破坏;
④烧碱熔化时,NaOH电离出钠离子和氢氧根离子,离子键被破坏;
⑤氯化氢溶于水,氯化氢在水分子的作用下电离出氢离子和氯离子,共价键被破坏;
⑥氯化铵受热分解生成氨气和氯化氢,离子键和共价键被破坏;
(1)通过以上分析知,化学键没有被破坏的是①②;仅发生离子键破坏的是③④;正确答案:①②;③④。
(2)既发生离子键又发生共价键破坏的是⑥;正确答案:⑥。
(3)氮气为共价分子,氮氮原子间形成三对共用电子对,其电子式为![]() ;Na2O2为离子化合物,钠离子和过氧根离子间为离子键,其电子式为
;Na2O2为离子化合物,钠离子和过氧根离子间为离子键,其电子式为![]() ;CO2为共价化合物,碳氧原子间形成双键,其电子式为
;CO2为共价化合物,碳氧原子间形成双键,其电子式为![]() ;正确答案:
;正确答案:![]() ;
; ![]() ;
; ![]() 。
。
(4)金属镁失电子,变为镁离子;氯原子得电子变为氯离子,电子式表示MgCl2的形成过程为:![]() ;正确答案:
;正确答案:![]() 。
。
(5)在反应N2+3H2=2NH3中,断裂3molH-H键,1molN≡N键共吸收的能量为:3×436+946=2254kJ,生成2molNH3,共形成6molN-H键,放出的能量为:6×391=2346 kJ,吸收的能量少,放出的能量多,该反应为放热反应,生成2molNH3放出的热量为:2346-2254=92 kJ,所以生成1molNH3放出的热量为92/2=46 kJ ;正确答案: 46 kJ。


 小题狂做系列答案
小题狂做系列答案科目:高中化学 来源: 题型:
【题目】我国已跨入“互联网+”时代,而“互联网+”的建设离不开无机非金属材料硅。下列物品中用到硅单质的是( )
A.计算机芯片B.陶瓷餐具C.石英钟表D.光导纤维
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】芳香化合物在催化剂催化下与卤代烃发生取代反应称为Friedel-Crafts烷基化反应。某科研小组以苯和氯代叔丁烷[ClC(CH3)3]为反应物,无水AlCl3为催化剂条件下制备叔丁基苯(![]() )。反应如下:
)。反应如下:
![]() 。
。
已知:
(1)AlCl3:熔点:190 C,沸点:180 C,遇水极易潮解并产生白色烟雾,微溶于苯。
(2)苯:M=78g/mol,ρ:0.88g/cm3,沸点:80.1 C,难溶于水,易溶于乙醇。
(3)氯代叔丁烷M=92.5g/mol,ρ:1.84g/cm3,沸点:51.6 C,难溶于水,可溶于苯。
(4)叔丁基苯:M=134g/mol,ρ:0.87g/cm3,沸点:169 C,难溶于水,易溶于苯。
I、如图是实验室制备无水AlCl3的实验装置:
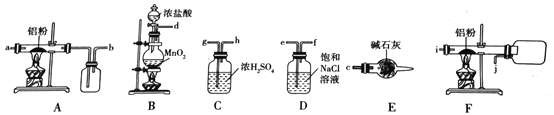
(1)选择合适的装置制备无水AlCl3正确的连接顺序为:_____________________(写导管口标号)。
(2)写出B装置中发生反应的离子方程式:______________。
(3)能否将E装置替换成C装置:______(填“能”或“不能”)理由:__________。
II、实验室制取叔丁基苯装置如图:

在三颈烧瓶中加入50mL的苯和适量的无水AlCl3,由恒压漏斗滴加氯代叔丁烷[ClC(CH3)3]10mL,一定温度下反应一段时间,将反应后的混合物依次用稀盐酸、5%Na2CO3溶液、H2O洗涤分离,在所得产物中加入少量无水MgSO4固体,静置,过滤,蒸馏得叔丁基苯20g。
(4)仪器A的名称为_______,B中试剂是碱石灰,其作用是_____________________,使用恒压漏斗的优点是__________________________。
(5)用H2O洗涤的目的是______________,加无水MgSO4固体的作用是______________。
(6)叔丁基苯的产率为____________。(保留3位有效数字)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硬脂酸甘油酯在碱性条件下水解的装置如图所示。进行皂化反应时的步骤如下:
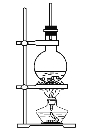
(1)在圆底烧瓶中装入7~8 g硬脂酸甘油酯,然后加入2~3 g的氢氧化钠、5 mL水、10 mL酒精。加入酒精的作用为______________________;
加入NaOH溶液的作用是___________________________。
(2)隔着石棉网给反应混合物加热约10 min,皂化反应基本完成。证明皂化反应进行完全的方法是_______________________。
(3)皂化反应完成后,加入饱和NaCl溶液的作用是____________________。
(4)图中长玻璃导管的作用为________________________。
(5)写出该反应的化学方程式:_________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某中学化学兴趣小组对乙醇的分子结构进行探究,其过程如下:
猜想一:乙醇的结构简式是CH3CH2OH
猜想二:乙醇的结构简式是CH3OCH3
制定方案并实施:按下图所示实验装置进行实验,

测定乙醇与钠反应(放热)生成氢气的体积,并据此计算乙醇分子中能与金属钠反应的氢原子的数目。
试回答下列问题:
(1)指出实验装置中的错误 。
(2)如果实验装置和操作正确,且结论符合猜想一,则参加反应的乙醇的物质的量与产生氢气的物质的量之比可能为 。
(3)如果实验装置和操作正确,且结论符合猜想二,则参加反应的乙醇的物质的量与产生氢气的物质的量之比可能为 。
(4)如果实验装置正确,实验结果为2.3 g乙醇与足量金属钠反应时产生了标准状况下的氢气约0.56 L,则乙醇的结构简式应为 ,理由是 。
(5)该实验获得成功的关键,除了需要纠正图中的装置错误以外,还需注意下列问题中的 (用序号填写)。
①装置的气密性良好;
②实验开始前准确测定乙醇的量;
③钠足量;
④广口瓶中水的体积大于560 mL;
⑤氢气的体积测算准确。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某气态烃在标准状况下密度为2.59 g·L-1。
(1)其相对分子质量等于________。
(2)该烃的含碳量为82.8%,则分子中碳、氢原子的个数比是________,分子式是________。
(3)可能的结构简式及名称是______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化合物的化学式为(NH4)2Fe(SO4)2 ,它在水溶液里电离时生成两种阳离子和一种酸根离子
(1)写出硫离子的结构示意图________________;
(2)若向该化合物的水溶液中通入氯气,一种离子很容易被氧化,该离子将变成______;(用离子符号表示)
(3)若向该化合物的水溶液中加入过量一种碱溶液,只能发生一个离子反应,则该反应的离子方程式为__________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com