
| A. |  | B. | 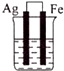 | C. | 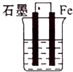 | D. |  |
 活力课时同步练习册系列答案
活力课时同步练习册系列答案科目:高中化学 来源: 题型:解答题
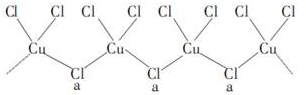
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 把钠投入水中:Na+2H2O═Na++2OH-+H2↑ | |
| B. | 向海带灰浸出液中加入硫酸、双氧水:2I-+2H++H2O2═I2+2H2O | |
| C. | 碳酸氢钠与稀硫酸反应:CO32-+2H+═H2O+CO2↑ | |
| D. | 向NaAlO2溶液中通入过量CO2:2AlO2-+CO2+3H2O═2Al(OH)3↓+CO32- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
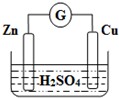
| A. | Zn是负极,Cu是正极 | B. | 稀硫酸溶液中H+移向Zn极 | ||
| C. | 电子由铜片通过导线流向锌片 | D. | 该装置能将电能转变为化学能 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1mol Cl2参加反应转移电子数一定为2NA | |
| B. | 常温常压下,NA个CH4分子占有的体积约为22.4L | |
| C. | 常温常压下,1mol Na2O2中阴离子为2NA个 | |
| D. | 标准状况下,11.2L16O2和11.2L18O2均含有NA个氧原子 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| t/min | 0 | 2 | 4 | 6 |
| V( 02 )/mL | 0.0 | 9.9 | 17.2 | 22.4 |
| A. | 0-2min的平均反应速率比4-6min快 | |
| B. | 0-6min 的平均反应速率v( H2O2)=3.3 x 10-2 moL-1•min-1 | |
| C. | 反应至 6min 时,c( H2O2)=0.3mol•L-1 | |
| D. | 反应至6min时,H2O2分解了 50% |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 4.6 g乙醇中含有的C-H键的个数为0.6NA | |
| B. | 34 gH2O2中含有的阴离子数为NA | |
| C. | 标准状况下,11.2 LCHCl3中含有的分子数为0.5NA | |
| D. | 9.2gNO2和N2O4混合气体中含有的原子总数为0.6NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | “血液透析”利用了胶体的性质 | |
| B. | 铜盐溶液都有毒,Cu2+能使蛋白质变性 | |
| C. | 硅酸钠的水溶液俗称水玻璃,是制备硅胶和木材防火剂等的原料 | |
| D. | 漂白液的有效成分为CaCl2和Ca(ClO)2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com