
| A.1000mL,212g | B.950mL,201.4g |
| C.500mL,286g | D.任意规格,572g |
科目:高中化学 来源:不详 题型:问答题
| 应取浓硫酸的体积/ml | 应选用容量瓶的规格/mL | 除容量瓶外还需要的其它仪器 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题
查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题
查看答案和解析>>
科目:高中化学 来源:不详 题型:多选题
| A.称量12.8gCuSO4固体,在100mL烧杯中加入80mL蒸馏水充分溶解 |
| B.称量20gCuSO4?5H2O固体,用80mL容量瓶配制成溶液 |
| C.用容量瓶配制溶液过程中,玻璃棒起搅拌加速溶解和引流液体的作用 |
| D.当用胶头滴管定容时,若视线偏低,则所配制的溶液浓度偏低 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题
查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题
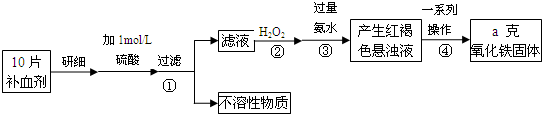
查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题
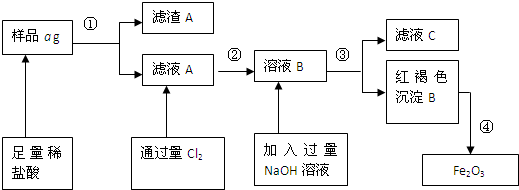
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com