
| A. | 硫酸铝的电离方程式:Al2(SO4)3=2Al3++3SO42- | |
| B. | 小苏打的电离方程式:NaHCO3=Na++H++CO32- | |
| C. | Mg(OH)2难溶于水,所以Mg(OH)2不是电解质,而是非电解质 | |
| D. | K2CO3溶液能导电,所以K2CO3溶液是电解质 |
分析 A.硫酸铝强电解质,完全电离出铝离子和硫酸根离子;
B.NaHCO3是弱酸的酸式盐,氢离子不能拆开;
C.酸碱盐都是电解质;
D.溶液是混合物,不是电解质.
解答 解:A.硫酸铝强电解质,完全电离出铝离子和硫酸根离子,则硫酸铝的电离方程式:Al2(SO4)3=2Al3++3SO42-,故A正确;
B.NaHCO3是弱酸的酸式盐,氢离子不能拆开,小苏打的电离方程式:NaHCO3=Na++HCO3-,故B错误;
C.酸碱盐都是电解质,Mg(OH)2属于碱,是电解质,故C错误;
D.K2CO3溶液中存在能自由移动的离子,能导电,溶液是混合物,不是电解质,电解质都是纯净物,故D错误.
故选A.
点评 本题考查了电解质的电离方程式、电解质的判断,题目难度不大,注意把握电解质的概念以及电离方程式的书写方法,侧重于考查学生对基础知识的应用能力.


 世纪百通期末金卷系列答案
世纪百通期末金卷系列答案科目:高中化学 来源: 题型:选择题
| A. | 用敞口容器称量NaOH且时间过长 | |
| B. | 定容时俯视读取刻度 | |
| C. | 原容量瓶洗净后未干燥 | |
| D. | 配制过程中,未用蒸馏水洗涤烧杯和玻璃棒 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
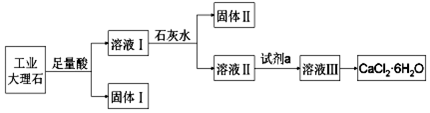
| A. | 固体Ⅰ中含有SiO2 | |
| B. | 使用石灰水时,要控制pH,防止固体Ⅱ中Al(OH)3转化为[Al(OH)4]- | |
| C. | 试剂a选用盐酸,从溶液Ⅲ得到CaCl2•6H2O的过程中,须控制条件防止其分解 | |
| D. | 若改变实验方案,在溶液Ⅰ中直接加氨水至沉淀完全,滤去沉淀,其溶液经蒸发浓缩、冷却结晶也可得到纯净CaCl2•6H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 按系统命名法,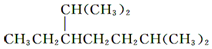 的名称为2,6二甲基5乙基庚烷 的名称为2,6二甲基5乙基庚烷 | |
| B. | 丙氨酸和甘氨酸脱水,最多可生成4种二肽 | |
| C. | 化合物 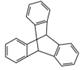 是芳香族化合物 是芳香族化合物 | |
| D. | 三硝酸甘油酯的分子式为C3H5N3O9 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 漂白粉的有效成分是Ca(ClO)2和CaCl2 | |
| B. | 漂白粉在空气中久置后会变质 | |
| C. | 漂白粉是由Cl2与烧碱制得的 | |
| D. | 在使用漂白粉时应用浓盐酸 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com