
 ��
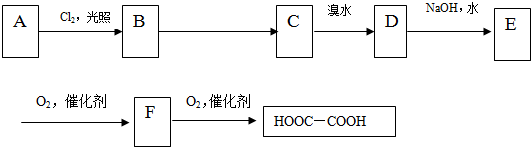
�� ���� A��CH3CH3��B����Է���������A��34.5����A����������ȡ����Ӧ����B����B��CH3CH2Cl��B���������ƵĴ���Һ������ȥ��Ӧ������ϩ����C��CH2=CH2��F����������HOOC-COOH����F��OHC-CHO��E��������OHC-CHO����E��CH2OHCH2OH��C���巢���ӳɷ�Ӧ����D��D���������Ƶ�ˮ��Һ����ȡ����Ӧ����E����D��CH2BrCH2Br���ݴ˷������
��� �⣺A��CH3CH3��B����Է���������A��34.5����A����������ȡ����Ӧ����B����B��CH3CH2Cl��B���������ƵĴ���Һ������ȥ��Ӧ������ϩ����C��CH2=CH2��F����������HOOC-COOH����F��OHC-CHO��E��������OHC-CHO����E��CH2OHCH2OH��C���巢���ӳɷ�Ӧ����D��D���������Ƶ�ˮ��Һ����ȡ����Ӧ����E����D��CH2BrCH2Br��
��1���������Ϸ�����B��CH3CH2Cl��E��CH2OHCH2OH��F��OHC-CHO��
�ʴ�Ϊ��CH3CH2Cl��CH2OH-CH2OH��OHC-CHO��
��2���������Ϸ�����A��B��ȡ����Ӧ��B��C����ȥ��Ӧ��E��F��������Ӧ��
�ʴ�Ϊ��ȡ����Ӧ����ȥ��Ӧ��������Ӧ��
��3��B��C��B���������ƵĴ���Һ������ȥ��Ӧ������ϩ����Ӧ����Ϊ���������ƴ���Һ�����ȣ�
�ʴ�Ϊ���������ƴ���Һ�����ȣ�
��4��D��CH2BrCH2Br��CH2BrCH2Br���������Ƶ�ˮ��Һ�ڼ��������·���ȡ����Ӧ����CH2OHCH2OH����Ӧ����ʽΪ��CH2BrCH2Br+2NaOH $��_{��}^{H_{2}O}$CH2OHCH2OH+2NaBr��
�ʴ�Ϊ��CH2BrCH2Br+2NaOH $��_{��}^{H_{2}O}$CH2OHCH2OH+2NaBr��
��5��CH2OH-CH2OH��������OHC-CHO����Ӧ�Ļ�ѧ����ʽΪ��CH2OH-CH2OH+O2 $��_{��}^{Cu}$ OHC-CHO+2H2O��
�ʴ�Ϊ��CH2OH-CH2OH+O2 $��_{��}^{Cu}$ OHC-CHO+2H2O��
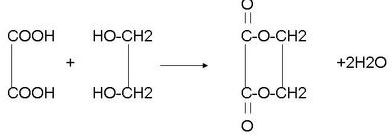
��6��EΪCH2OHCH2OH����HOOC-COOH������Ӧ���ɻ�״���Ӧ�ķ���ʽΪ�� ��
��
�ʴ�Ϊ�� ��
��
���� ���⿼�����л�����ƶϣ���Ŀ�Ѷ��еȣ���HOOC-COOHΪͻ�ƿڲ������Ƶķ��������ƶϣ���ȷ�л���Ľṹ�������ǽⱾ��ؼ���ע�ⷴӦ��������Ӧ������ͬ���²��ﲻͬ��Ϊ�״��㣬����������ѧ���ķ���������������������



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | С�մ����������۷��� | B�� | SO2������Ư��ֽ�� | ||
| C�� | BaCO3��ҽѧ���������� | D�� | �����ڳ�ȥůˮƿ�е�ˮ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
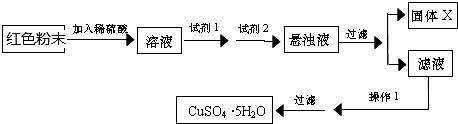
| ���� | Cu��OH��2 | Fe��OH��2 | Fe��OH��3 |
| ��ʼ����pH | 6.0 | 7.5 | 1.4 |
| ������ȫpH[���� | 13 | 14 | 3.7 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | CH3COOH+OH-�TCH3COO-+H2O | B�� | H++OH-�TH2O | ||
| C�� | CH3COOH+OH-+Na+�TCH3COONa+H2O | D�� | CH3COOH+NaOH�TCH3COO-+Na++H2O |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

 ��
��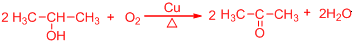 ��
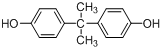
��
 ��
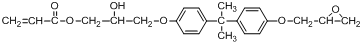
��
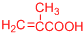 ����
����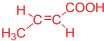 ��
��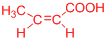 ����
�����鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
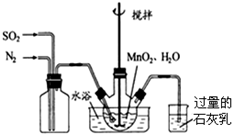
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �������;ƾ� | B�� | �屽���� | C�� | �ױ���ˮ | D�� | �������ͼ��� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com