
【题目】己知重铬酸钾在水溶液中存在如下平衡:2CrO42-(黄色)+2H+![]() Cr2O72-(橙红色)+H2O。下列说法正确的是
Cr2O72-(橙红色)+H2O。下列说法正确的是
A. 当溶液的pH降低时,平衡向左移动
B. 恒温下,将上述溶液用蒸馏水稀释到原体积的2倍,平衡向右移动
C. 当溶液颜色不变时,溶液的c(H+)/c(OH-)是一个定值
D. 增大CrO42-浓度,平衡向右移动,平衡常数增大
 计算高手系列答案
计算高手系列答案科目:高中化学 来源: 题型:
【题目】某烃A是有机化学工业的基本原料,其产量可以用来衡量一个国家的石油化工发展水平,A还是一种植物生长调节剂,A可发生如图所示的一系列化学反应,其中①②属于同种反应类型。根据图回答下列问题:
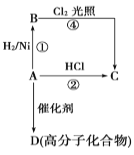
(1)写出A、B、C、D的结构简式:A______,B_______,C_______,D_______。
(2)写出②、④两步反应的化学方程式,并注明反应类型:
②______________,反应类型___________。
④______________,反应类型___________。
(3)工业上制取A的主要方法是_____,实验室制取A的反应条件是______,实验室制取A时,会生成黑色固体,并放出刺激性气味的气体,检验该气体可以用______溶液;黑色固体与浓硫酸反应产生该气体时,体现了浓硫酸的_____性
(4)D_____(填“有”或“没有”)固定熔点。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学设计了一组电化学装置如图所示,其中乙装置中 X 为阳离子交换膜,甲醇(CH3OH)具有可燃性。
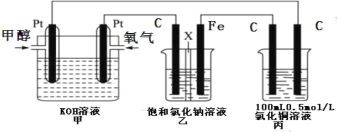
根据要求回答相关问题:
(1)写出装置甲中负极的电极反应式:________。
(2)装置乙中石墨电极(C)的电极反应式为:_________。
(3)当装置甲中消耗 0.05molO2 时,丙装置中阳极产生气体的体积 ____________L(标况下);
(4)若按(3)数据,装置乙中溶液的 pH 为_____________(溶液体积为 200mL 不变)。要使乙中溶液恢复到原来的状态,需要加入的物质是__________,对应用量为___________mol.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】阿巴卡韦(Abacavir) 是一种核苷类逆转录酶抑制剂,存在抗病毒功效。关于其合成中间体M(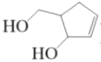 ),下列说法正确的是
),下列说法正确的是
A.与环戊醇互为同系物B.分子中所有碳原子共平面
C.和1 mol 钠反应可以生成 22.4 L 氢气D.可用碳酸氢钠溶液鉴别乙酸和M
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CO2的回收与利用是科学家研究的热点课题。可利用CH4与CO2制备合成气(CO、H2),还可制备甲醇、二甲醚、低碳烯经等燃料产品。
I.科学家提出制备“合成气”反应历程分两步:
反应①:CH4(g)C(ads) +2H2(g) (慢反应)
反应②:C(ads) + CO2(g)2CO(g) (快反应)
上述反应中C(ads)为吸附性活性炭,反应历程的能量变化如图:
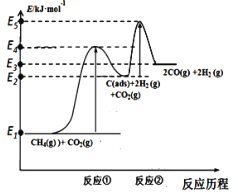
(1)CH4与CO2制备合成气的热化学方程式为____________:该反应在高温下可自发正向进行的原因是_________,能量变化图中:E5+E1___E4+E2(填“>”、“<”或“=”)。
II.利用“合成气”合成申醇后,脱水制得二甲醚。
反应为:2CH3OH(g)CH3OCH3 (g) + H2O(g) △H
经查阅资料,在一定范围内,上述反应化学平衡常数与热力学温度存在如下关系:lnKc=-2.205+![]() 。其速率方程为:v正=k正c2(CH3OH),v逆=k逆c(CH3OCH3)c(H2O),k正、K逆为速率常数,且影响外因只有温度。
。其速率方程为:v正=k正c2(CH3OH),v逆=k逆c(CH3OCH3)c(H2O),k正、K逆为速率常数,且影响外因只有温度。
(2)反应达到平衡后,仅升高温度,k正增大的倍数________ k逆增大的倍数(填“>”、“<”或“= ”)。
(3)某温度下,Kc=200,在密闭容器中加入一定量CH3OH。反应到某时刻测得各组分的物质的量如下:
物质 | CH3OH | CH3OCH3 | H2O |
物质的量/mol | 0.4 | 0.4 | 0.4 |
此时正、逆反应速率的大小:v正 ____v逆(填“>”、“<”或“=”)。
(4)500K下,在密闭容器中加入一定量甲醇CH3OH,反应到达平衡状态时,体系中CH3OCH3(g)的物质的量分数为_____(埴标号)
A.![]() B.
B.![]() C.
C.![]() D.无法确定
D.无法确定
Ⅲ.合成低碳烯经
(5)强碱性电催化还原CO2制备乙烯研究取得突破进展,原理如图所示。b极接的是太阳能电池的_______极(已知PTFE浸泡了饱和KCl溶液)。请写出阴极的电极反应式______。
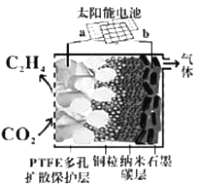
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为了探究金属单质M与盐溶液的反应,某同学进行了下列实验,实验过程及现象如图所示,结合实验现象判断该同学得出的下列结论中正确的是
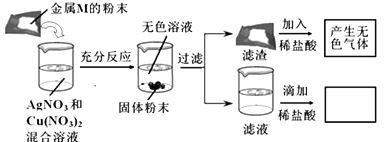
A. 向滤液中滴加盐酸的实验现象是产生白色沉淀
B. 滤渣可能是两种单质的混合物
C. 滤渣在足量的稀硝酸中能完全溶解
D. 加入的金属M可能是镁或钠
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】明矾[KA1(SO4)2·12H2O]是一种复盐,在造纸等方面应用广泛。采用废易拉罐制备明矾的过程如下图所示。
下列叙述错误的是
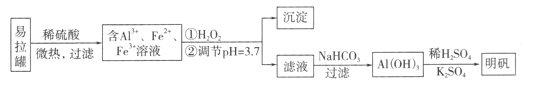
A. 合理处理易拉罐有利于环境保护和资源再利用
B. 从易拉罐中可回收的金属元素有Al、Fe
C. “沉淀”反应的金属离子为Fe3+
D. 上述流程中可用NaHSO4代替NaHCO3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学小组研究在其他条件不变时,改变密闭容器中某一条件对A2(g)+3B2(g)2AB3(g)化学平衡状态的影响,得到如图所示的曲线(图中T表示温度,n表示物质的量)下列判断正确的是
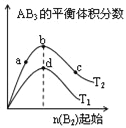
A. 图中T2一定大于T1
B. 图中b点速率一定大于d点速率
C. 达到平衡时,A2的转化率大小为:c>b>a
D. 加入催化剂可以使状态d变为状态b
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】温度为T时,向VL的密闭容器中充入一定量的A和B,发生反应:A(g)+B(g)![]() C(s)+xD(g) △H>0,容器中A、B、D的物质的量浓度随时间的变化如下图所示。下列说法中不正确的是
C(s)+xD(g) △H>0,容器中A、B、D的物质的量浓度随时间的变化如下图所示。下列说法中不正确的是
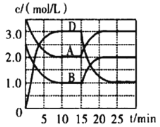
A.反应在前10min以B物质表示的平均反应速率v(B)=0.15 mol·L-1·min-1
B.该反应方程式中的x=2
C.若平衡时保持温度不变,压缩容器容积,平衡向逆反应方向移动
D.反应至15min时,改变的条件是降低温度
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com