
【题目】下列指定反应的离子方程式正确的是( )
A.向醋酸溶液中滴加浓氨水至过量:CH3COOH+OH-=CH3COO-+H2O
B.三氯化铁腐蚀印刷线路板:Fe3++Cu=Fe2++Cu2+
C.氧化亚铁与稀硝酸反应:FeO+2H+=Fe2++H2O
D.少量碳酸氢铵溶液与足量烧碱溶液混合加热:NH![]() +HCO
+HCO![]() +2OH-
+2OH-![]() NH3↑+CO
NH3↑+CO![]() +2H2O
+2H2O
科目:高中化学 来源: 题型:
【题目】设![]() 为阿伏加德罗常数的值,下列叙述错误的是( )
为阿伏加德罗常数的值,下列叙述错误的是( )
A.![]()
![]() 醋酸钠溶液含有的
醋酸钠溶液含有的![]() 数目为
数目为![]()
B.![]()
![]() 和
和![]() 的混合气体中含有
的混合气体中含有![]() 键的数目为
键的数目为![]()
C.7g乙烯和环丁烷![]() 的混合气体中含有的氢原子数目为
的混合气体中含有的氢原子数目为![]()
D.![]()
![]() 的浓
的浓![]() 与过量
与过量![]() 反应,转移的电子数大于
反应,转移的电子数大于![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质的转化在给定条件下能实现的是( )
①FeS2![]() SO2
SO2![]() H2SO4 ②SiO2
H2SO4 ②SiO2![]() SiCl4
SiCl4![]() Si
Si
③饱和NaCl溶液![]() NaHCO3
NaHCO3![]() Na2CO3 ④Al
Na2CO3 ④Al![]() NaAlO2
NaAlO2![]() Al(OH)3
Al(OH)3
⑤CuSO4(aq)![]() Cu(OH)2
Cu(OH)2![]() Cu2O
Cu2O
A. ①③⑤B. ②③④C. ②④⑤ D. ①④⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某品牌化妆品的主要成分Z具有美白功效,原从杨树中提取,现可用如下图所示反应合成。下列对X、Y、Z的叙述,正确的是
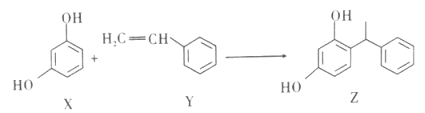
A. X、Y和Z均能和NaOH溶液反应
B. X和Z均能和Na2CO3溶液反应,但不能和NaHCO3溶液反应
C. Y既能发生加聚反应,也能发生缩聚反应
D. Y分子中所有原子不可能共平面
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室用H2还原WO3制备金属W的装置如图所示(Zn粒中往往含有硫等杂质,焦性没食子酸溶液用于吸收少量氧气),下列说法正确的是
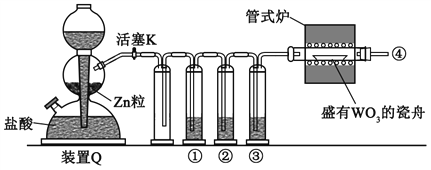
A. ①、②、③中依次盛装KMnO4溶液、浓H2SO4、焦性没食子酸溶液
B. 管式炉加热前,用试管在④处收集气体并点燃,通过声音判断气体纯度
C. 结束反应时,先关闭活塞K,再停止加热
D. 装置Q(启普发生器)也可用于二氧化锰与浓盐酸反应制备氯气
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物H是一种用于合成γ分泌调节剂的药物中间体,其合成路线流程图如下:
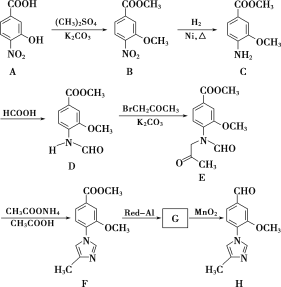
(1)C中的非含氧官能团名称为______。
(2)D→E 的反应类型为___________。
(3)写出A的一种羧酸同系物的结构简式: ____________。
(4)写出同时满足下列条件的![]() 的一种同分异构体的结构简式:_________。
的一种同分异构体的结构简式:_________。
①含有苯环,且苯环上只有2种不同化学环境的氢;
②属于α-氨基酸,且分子中有一个手性碳原子。
(5)G的分子式为C12H14N2O2 ,经氧化得到H,写出G的结构简式:_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】四苯基乙烯(TFE)及其衍生物具有诱导发光特性,在光电材料等领域应用前景广泛。以下是TFE的两条合成路线(部分试剂及反应条件省略):
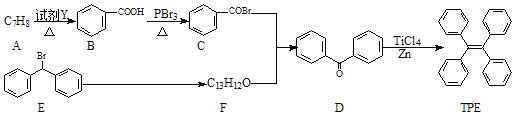
(1)A的名称是__;试剂Y为__。
(2)B→C的反应类型为__;B中官能团的名称是__,D中官能团的名称是__。
(3)E→F的化学方程式是___。
(4)W是D的同分异构体,具有下列结构特征:①属于萘(![]() )的一元取代物;②存在羟甲基(-CH2OH)。写出W所有可能的结构简式:__。
)的一元取代物;②存在羟甲基(-CH2OH)。写出W所有可能的结构简式:__。
(5)下列叙述正确的是__。
a.B的酸性比苯酚强
b.D不能发生还原反应
c.E含有3种不同化学环境的氢
d.TPE既属于芳香烃也属于烯烃
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:298K时,N2(g)+3H2(g)![]() 2NH3(g) △H=-92.2kJ·mol-1。
2NH3(g) △H=-92.2kJ·mol-1。
(1)若N≡N的键能为941.3kJ·mol-1,H—H的键能为436.4kJ·mol-1,则N—H的键能为___。
(2)实验室将1.1molN2、3molH2充入2L容器,一定条件下反应。保持温度和容器体积不变,
①若2min末测得H2的物质的量为1.8mol,则该时间段内氨气的平均反应速率为___。
②保持温度和容器体积不变,下列措施可加快该反应速率的是___。
A.充入He气
B.使用恰当的催化剂
C.升高反应体系的温度
D.再充入N2
③当下列物理量保持不变时,表明该反应一定处于化学平衡状态的是___。
A.容器内N2与H2的含量
B.容器内气体密度
C.恒温下容器的压强
D.H2的物质的量
(3)电化学气敏传感器可用于监测环境中NH3的含量,其工作原理如图所示:
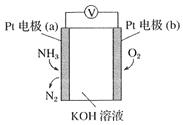
①外电路电流的运动方向:___。(填“a极到b极”或“b极到a极”)。
②b极电极反应式为___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将气体A、B置于固定容积为2 L的密闭容器中,发生如下反应:3A(g)+B(g)![]() 2C(g)+2D(g),反应进行到10 s末达到平衡,此时测得A的物质的量为1.8 mol,B的物质的量为0.6 mol,C的物质的量为0.8 mol。
2C(g)+2D(g),反应进行到10 s末达到平衡,此时测得A的物质的量为1.8 mol,B的物质的量为0.6 mol,C的物质的量为0.8 mol。
(1)用C表示10 s内反应的平均反应速率为________。
(2)10 s末,生成物D的浓度为________。
(3)A与B的平衡转化率之比为________。
(4)反应过程中容器内气体的平均相对分子质量变化是_____(填“增大”、“减小”或“不变”,下同),气体的密度变化是______。
(5)在一定温度下,体积不变的密闭容器中,上述反应达到平衡的标志是_______(填字母)。
A. 气体总质量保持不变 B. A、B、C、D的浓度都相等
C. 每消耗3 mol A的同时生成2 mol D D. A、B、C、D的分子数之比为3∶1∶2∶2
E. 3V正(A) = 2V逆(C) F. A的转化率保持不变
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com