
【题目】将紫色石蕊试液滴入NaOH溶液中,溶液变蓝色,再通入氯气,溶液由蓝色先变成红色,最后颜色慢慢褪去,其原因是( )
①氯气有漂白性 ②氯气与NaOH溶液反应 ③氯气的水溶液呈酸性 ④次氯酸有漂白性 ⑤氯化钠有漂白性
A.①④B.②③④C.①②③D.①⑤
科目:高中化学 来源: 题型:
【题目】有关分子结构如图所示,下列叙述中,正确的是 ( )
![]()
A. 除苯环外的其余碳原子有可能都在一条直线上
B. 所有的原子都在同一平面上
C. 12个碳原子不可能都在同一平面上
D. 12个碳原子有可能都在同一平面上
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表是周期表中的一部分,根据A-I在周期表中的位置,第(2) ~ (3)小题用元素符号或化学式回答,(4)~(6)小题按题目要求回答。
族 周期 | I A | Ⅱ A | Ⅲ A | Ⅳ A | Ⅴ A | Ⅵ A | Ⅶ A | O |
1 | A | |||||||
2 | D | E | G | |||||
3 | B | C | F | H | I |
(1)表中元素,化学性质最不活泼的原子结构示意图是___________,非金属性最强的元素在周期表中的位置是__________________________,
(2)最高价氧化物的水化物中碱性最强的是_________,酸性最强的是___________,
(3)A分别与D、E、G形成的最简单化合物中,最不稳定的_______________,
(4)A和E组成最简单化合物的电子______________
(5)在B、C、F、G的简单离子中,离子半径由大到小的顺序是__________________,
(6)由A的单质与O2构成的燃料电池中,在E的最高价氧化物对应水化物的条件下进行,写出正极的电极反应式______________________________________。
(7)当B的最高价氧化物的水化物与C的最高价氧化物反应后,向所得溶液中通入过量D的最高价氧化物的离子方程式___________________________________,
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为了确定某铝热剂(含氧化铁和铝)的组成,分别进行下列实验。
(1)若取a g样品,向其中加入足量的氢氧化钠溶液,测得生成的气体为b L(标况)。反应的离子方程式为_______________,样品中铝的物质的量为_____________(用含b的代数式表示)。
(2)若取a g样品,在高温下能恰好完全反应,该反应的化学方程式为________________,样品中氧化铁与铝的质量比为_________________(用含a 、b的代数式表示)。
(3)待(2)中反应产物冷却后,往其中加入足量的盐酸,测得生成的气体体积为c L(标况),则该气体与(1)中所得的气体的体积比c∶b=______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用质量分数为98%的浓硫酸(ρ=1.84 g·cm-3)配制240 mL 1.84 mol·L-1稀硫酸,下列操作正确的是( )
A. 将蒸馏水缓慢注入盛有一定量浓硫酸的烧杯中,并不断搅拌至冷却
B. 必需的定量仪器有100 mL量筒、250 mL容量瓶和托盘天平
C. 量取浓硫酸的体积为25.0 mL
D. 先在容量瓶中加入适量水,将量好的浓硫酸注入容量瓶,加水定容
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海带中含碘元素,有人设计如下步骤来提取碘:①通足量氯气 ②将海带烧成灰,向灰中加水搅拌 ③加入CCl4振荡 ④过滤 ⑤用分液漏斗分液.合理的操作顺序为( )
A.②﹣④﹣①﹣③﹣⑤
B.②﹣①﹣③﹣④﹣⑤
C.①﹣③﹣⑤﹣②﹣④
D.③﹣①﹣②﹣⑤﹣④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学欲用98%的浓H2SO4(ρ=1.84g/cm3)配制500mL 0.5molL﹣1的稀H2SO4。
(1)填写下列操作步骤:
①所需浓H2SO4的体积为______。
②如果实验室有10mL、20mL、50mL量筒,应选用______mL量筒量取。
③将量取的浓H2SO4沿内壁慢慢注入盛有约100m 水的烧杯里,并不断搅拌,目的是______。
④立即将上述溶液沿玻璃棒注入______中,并用50mL蒸馏水洗涤烧杯2~3次,并将洗涤液注入其中,并不时轻轻振荡。
⑤加水至距刻度线______处,改用______加水,使溶液的凹液面最低点正好跟刻度线相平。盖上瓶塞,上下颠倒数次,摇匀。
(2)请指出上述操作中一处明显错误______。
(3)误差请分析以下错误操作对所配制的溶液浓度的影响(填“偏高”“偏低”或“无影响”)。
①若进行操作⑤定容时,眼睛俯视,则所配制溶液的浓度将______。
②问题(2)的错误操作将导致所配制溶液的浓度______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是(设阿伏加德罗常数的数值为NA)( )
A.在标准状况下,22.4L水所含分子数目为NA
B.1molL﹣1 K2SO4溶液所含K+数目为2NA
C.1mol钠与氧气反应生成Na2O或Na2O2时,失电子数目均为NA
D.O2的摩尔体积约为22.4 Lmol﹣1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为减小CO2对环境的影响,在倡导“低碳”的同时,还需加强对CO2创新利用的研究。T1 ℃时,将9 mol CO2和12 mol H2充入3 L密闭容器中,发生反应CO2(g)+3H2(g) ![]() CH3OH(g)+H2O(g) ΔH<0,容器中CH3OH的物质的量随时间变化如曲线Ⅰ所示,平衡时容器内压强为p1。改变某一条件重新进行上述反应,CH3OH的物质的量随时间变化如曲线Ⅱ所示。下列说法错误的是
CH3OH(g)+H2O(g) ΔH<0,容器中CH3OH的物质的量随时间变化如曲线Ⅰ所示,平衡时容器内压强为p1。改变某一条件重新进行上述反应,CH3OH的物质的量随时间变化如曲线Ⅱ所示。下列说法错误的是
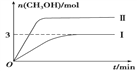
A. 曲线Ⅱ对应的条件改变是增大压强
B. T2 ℃时,上述反应平衡常数为0.42,则T2>T1
C. 在T1 ℃,若起始时向容器中充入5 mol CO2、5 mol H2、5 mol CH3OH(g)和5 mol H2O(g),则达平衡前v(正)>v(逆)
D. 在T1 ℃,若起始时向容器中充入4.5 mol CO2、6 mol H2,平衡时容器内压强p=![]()
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com