
设NA为阿伏加德罗常数的数值,下列说法正确的是()
A. 1mol某烷烃分子中含8 mol氢原子,则1 mol该烷烃分子中共价键数为8NA
B. 标准状况下,a L氧气和氮气的混合物中含有的分子数为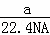
C. 1.4g乙烯分子中含有0.05NA个C=C键
D. 1mol Cl2发生反应时,转移的电子数一定是2NA
考点: 阿伏加德罗常数.
专题: 阿伏加德罗常数和阿伏加德罗定律.
分析: A.1mol烷烃分子中含有8mol氢原子,则该烷烃为丙烷,丙烷分子中含有8mol碳碳键和2mol碳碳键,总共含有10mol共价键;
B.标况下aL混合气体的物质的量为 =
= mol;
mol;
C.乙烯分子中含有1个碳碳双键,1.4g乙烯的物质的量为0.05mol,含有0.05mol碳碳双键;
D.1mol氯气与氢氧化钠溶液反应时得到了1mol电子.
解答: 解:A.1mol烷烃分子中含有8mol氢原子,该烷烃为丙烷,丙烷中含有8molC﹣H共价键、2molC﹣C键,总共含有10mol共价键,含有的共价键数为10NA,故A错误;
B.标准状况下,aL氧气和氮气混合气体的物质的量为: =
= mol,含有的分子数为
mol,含有的分子数为 NA,故B错误;
NA,故B错误;
C.1.4g乙烯的物质的量为0.05mol,0.05mol乙烯分子中含有0.05mol碳碳双键,含有0.05NA个C=C键,故C正确;
D.1molCl2发生反应时,如果与氢氧化钠溶液反应,1mol氯气得到了1mol电子,转移电子数一定是NA,故D错误;
故选C.
点评: 本题考查阿伏加德罗常数的有关计算和判断,题目难度中等,注意掌握好以物质的量为中心的各化学量与阿伏加德罗常数的关系,选项D为易错点,注意氯气与氢氧化钠溶液的反应中,氯气既是氧化剂,也是还原剂.


科目:高中化学 来源: 题型:
硫酸钙是一种用途非常广泛的产品,可用于生产硫酸、漂白粉等一系列物质(见图).下列说法正确的是()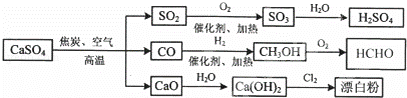
A. CO、SO2、SO3均是酸性氧化物
B. 除去与水反应,图示转化反应均为氧化还原反应
C. 工业上利用Cl2和澄清石灰水反应来制取漂白粉
D. 用CO合成CH3OH进而合成HCHO的两步反应,原子利用率均为100%
查看答案和解析>>
科目:高中化学 来源: 题型:
对实验Ⅰ~Ⅳ的实验现象预测正确的是()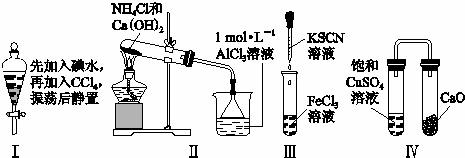
A. 实验Ⅰ:液体分层,下层呈无色
B. 实验Ⅱ:烧杯中先出现白色沉淀,后溶解
C. 实验Ⅲ:试管中产生血红色沉淀
D. 实验Ⅳ:放置一段时间后,饱和CuSO4溶液中出现蓝色晶体
查看答案和解析>>
科目:高中化学 来源: 题型:
设NA为阿伏加德罗常数的数值,下列叙述中完全正确的一组是( )
①常温常压下,1mol甲基(﹣CH3)所含的电子数为10NA
②由Cu、Zn和稀硫酸组成的原电池工作时,若Cu极生成0.2gH2,则电路中通过电子0.2NA
③5.6g铁粉与硝酸反应失去的电子数一定是0.3NA
④常温常压下,16gO2和O3的混合物中所含的原子数为NA
⑤1molC10H22分子中共价键总数为31NA
⑥1molCl2发生反应时,转移的电子数一定是2NA.
A. ②③④ B. ②③⑥ C. ①②④⑤ D. ②④⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
A~E是中学常见的5种化合物,A、B是氧化物,它们之间的转化关系如图所示.则下列说法正确的是()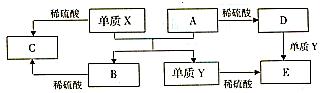
A. x与A反应的化学方程式是:Al2O3+2Fe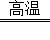 Fe2O3+2Al
Fe2O3+2Al
B. 检验D溶液中的金属阳离子的反应:Fe3++3SCN﹣=Fe(SCN)3↓
C. 单质Y在一定条件下能与水发生置换反应
D. 由于化合物B和C均既能与酸反应,又能与碱反应,所以均是两性化合物
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com