
| 序号 | 矿石粒度/目 | 钴浸出率/% |
| 1 | -60 | 9.8 |
| 2 | -120 | 25.5 |
| 3 | -200 | 41.18 |
 .
.
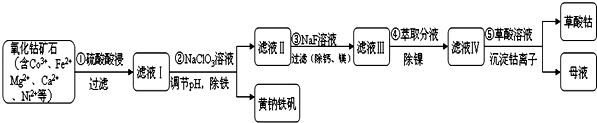
分析 氧化钴矿石制取CoC2O4(草酸钴),含有Co3+、Fe2+、Mg2+、Ca2+、Ni2+,黄钠铁矾不溶于水,可溶于酸,加入硫酸酸浸过滤得到滤液Ⅰ加入NaClO3溶液调节溶液PH除去Fe3+生成氢氧化铁沉淀除去,过滤得到滤液Ⅱ,加入NaF除去Mg2+、Ca2+离子,过滤得到滤液Ⅲ,加入萃取剂除去Ni2+,得到滤液Ⅳ中加入草酸溶液沉淀钴离子过滤得到草酸钴,
(1)矿石粒度对钴浸出率的影响可知,选择矿石粒度应使浸出率最高;
(2)步骤①是过滤装置,据此分析需要用到的玻璃仪器;
(3)NaClO3将Fe2+氧化成Fe3+,酸溶液中氯酸根离子被还原为氯离子,结合离子电荷守恒,原子守恒、电子守恒配平书写化学方程式,标注电子转移;
(4)步骤 ③中除去镁离子的反应是氟离子和镁离子结合生成氟化镁沉淀;
(5)取黄钠铁矾用盐酸溶液溶解,分成两份,一份用焰色反应检验钠元素的存在,另一份检验铁离子的存在;
(6)母液中硫酸钴和草酸反应生成草酸钴沉淀和硫酸,参与反应最后又生成的物质可以循环使用.
解答 解:氧化钴矿石制取CoC2O4(草酸钴),含有Co3+、Fe2+、Mg2+、Ca2+、Ni2+,黄钠铁矾不溶于水,可溶于酸,加入硫酸酸浸过滤得到滤液Ⅰ加入NaClO3溶液调节溶液PH除去Fe3+生成氢氧化铁沉淀除去,过滤得到滤液Ⅱ,加入NaF除去Mg2+、Ca2+离子,过滤得到滤液Ⅲ,加入萃取剂除去Ni2+,得到滤液Ⅳ中加入草酸溶液沉淀钴离子过滤得到草酸钴,
(1)矿石粒度对钴浸出率的影响可知,选择矿石粒度应使浸出率最高,矿石粒度为-200目,钴浸出率41.18%,浸出率最高,
故答案为:-200;
(2)步骤①是过滤装置,据此分析需要用到的玻璃仪器,用到的玻璃仪器,除烧杯外还有漏斗、玻璃棒,
故答案为:漏斗、玻璃棒;
(3)NaClO3将Fe2+氧化成Fe3+,酸溶液中氯酸根离子被还原为氯离子,结合离子电荷守恒,原子守恒、电子守恒配平书写化学方程式,标注电子转移,得到的离子方程式为: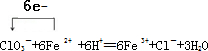 ,
,
故答案为: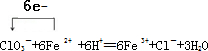 ;
;
(4)步骤 ③中除去镁离子的反应是氟离子和镁离子结合生成氟化镁沉淀,反应的离子方程式为:Mg2++2F-=MgF2↓,
故答案为:Mg2++2F-=MgF2↓;
(5)取黄钠铁矾用盐酸溶液溶解,分成两份,一份用焰色反应检 验钠元素的存在,另一份检验铁离子的存在,实验设计为:取黄钠铁矾用盐酸溶液溶解,分成两份,一份做火焰色反应,火焰为黄色证明有Na+存在;另一份向其中滴加KSCN溶液,溶液变成血红色,证明有Fe3+存在,
故答案为:取黄钠铁矾用盐酸溶液溶解,分成两份,一份做火焰色反应,火焰为黄色证明有Na+存在;另一份向其中滴加KSCN溶液,溶液变成血红色,证明有Fe3+存在;
(6)母液中硫酸钴和草酸反应生成草酸钴沉淀和硫酸,参与反应最后又生成的物质可以循环使用,硫酸可以循环使用,
故答案为:硫酸.
点评 本题考查了物质分离提纯,物质性质和实验分离方法、流程的分析应用,主要是物质性质的理解应用,掌握基础是解题关键,题目难度中等.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 实施以减少能源浪费和降低废气排放为基本内容的节能减排政策,是应对全球气候问题、建设资源节约型、环境友好型社会的必然选择.化工行业的发展必须符合国家节能减排的总体要求.试运用所学知识,解决下列问题:
实施以减少能源浪费和降低废气排放为基本内容的节能减排政策,是应对全球气候问题、建设资源节约型、环境友好型社会的必然选择.化工行业的发展必须符合国家节能减排的总体要求.试运用所学知识,解决下列问题: CO(g)+H2(g)△H=+132kJ/mol
CO(g)+H2(g)△H=+132kJ/mol| 温度/℃ | 400 | 500 | 800 |
| 平衡常数K | 9.94 | 9 | 1 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 实验序号 |  | 0 | 10 | 20 | 30 | 40 | 50 |
| 1 | 500 | 2.0 | 1.6 | 1.3 | 1.0 | 0.8 | 0.8 |
| 2 | 500 | C2 | 1.2 | 0.8 | 0.8 | 0.8 | 0.8 |
| 3 | 500 | C3 | 1.7 | 1.3 | 1.0 | 1.0 | 1.0 |
| 4 | 600 | 2.0 | 1.1 | 0.9 | 0.9 | 0.9 | 0.9 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 3:2:2 | B. | 1:2:3 | C. | 1:3:3 | D. | 3:1:1 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com