
A、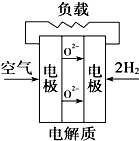 |
B、 |
C、 |
D、 |


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、分液、萃取、蒸馏 |
| B、萃取、蒸馏、分液 |
| C、分液、蒸馏、萃取 |
| D、蒸馏、萃取、分液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、FeCl3溶液中:H+、Na+、Cl-、H2O2 | ||||
| B、酸性KMnO4的溶液中:Na+、NO3-、K+、CH3CH2OH | ||||
| C、混有氯化氢气体的氯气中:O2、CH4、N2、NH3 | ||||
D、c(H+)=0.10mol/L的溶液中:NH
|
查看答案和解析>>
科目:高中化学 来源: 题型:
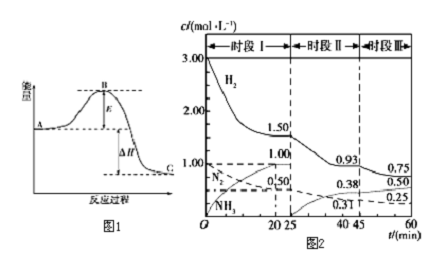
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、需要加热方能发生的反应一定是吸热反应 |
| B、放热的反应在常温下一定很容易发生 |
| C、反应是放热还是吸热,取决于反应物和生成物所具有的总能量的相对大小 |
| D、伴有能量变化的物质变化都是化学变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、用25mL量筒量取22.30mL盐酸 |
| B、用托盘天平称量8.75g食盐 |
| C、将20gNa2CO3溶于80g水中制得20%的Na2CO3溶液 |
| D、将标准状况下22.4LHCl气体溶于1L水中可制得1mol/L盐酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
| A、CO的燃烧热为566.0 kJ?mol-1 |
| B、2 mol CO和1 mol O2的总能量比2 mol CO2的总能量低 |
| C、完全燃烧20g甲醇,生成二氧化碳和水蒸气时放出的热量为908.3 kJ |
| D、2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(g)△H=-1453.28 kJ?mol-1 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com