
比较1.0 mol N2和1.0 mol CO的:①质量 ②分子总数 ③原子总数,其中相同的是( )
A.① B.①②
C.①②③ D.②③
 暑假作业海燕出版社系列答案
暑假作业海燕出版社系列答案 本土教辅赢在暑假高效假期总复习云南科技出版社系列答案
本土教辅赢在暑假高效假期总复习云南科技出版社系列答案科目:高中化学 来源: 题型:
下列叙述中不正确的是( )
A.“氯碱工业”通过电解饱和食盐水生产氯气和烧碱。
B.通常状况下,干燥的氯气能和Fe反应
C.纯净的H2在Cl2中安静地燃烧,发出苍白色火焰,集气瓶口呈现雾状;光照H2和Cl2的混合气体时,因迅速化合而爆炸
D.新制氯水具有漂白性,久置氯水最终变为稀盐酸
查看答案和解析>>
科目:高中化学 来源: 题型:
铜和浓硫酸发生反应的化学方程式为:
Cu +2H2SO4(浓)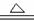 CuSO4+SO2↑+2H2O,其中硫元素被________
CuSO4+SO2↑+2H2O,其中硫元素被________
(填“氧化”或“还原”,下同),发生 反应;浓H2SO4作_________剂,具有 性。在该反应中,若消耗了32 g Cu,则转移了_______mol 电子 ,生成 L SO2(标准状况)气体。
查看答案和解析>>
科目:高中化学 来源: 题型:
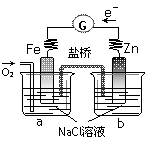
根据右图,下列判断正确的是
A.电子从Zn极流出,流入Fe极,经盐桥回到Zn极
B.烧杯a中发生反应O2+4H++4e-=2H2O,溶液pH升高
C.烧杯b中发生的电极反应为Zn-2e-=Zn2+
D.向烧杯a中加入少量K3Fe(CN)6溶液,有蓝色沉淀生成
查看答案和解析>>
科目:高中化学 来源: 题型:
Li-SOCl2电池是一种新型电池。该电池的电极材料分别为锂和碳,电解液是LiAlCl4—SOCl2。电池的总反应可表示为:4Li+2SOCl2 = 4LiCl +S +SO2。
(1)电池正极发生的电极反应为 ;
(2)SOCl2易挥发,实验室中常用NaOH溶液吸收SOCl2,有Na2SO3和NaCl生成。 如果把少量水滴到SOCl2中,反应的化学方程式为 ;
(3)用Li-SOCl2电池在实验室条件下以硫酸铜溶液为电解液,用电解的方法实现了粗铜(含有少量的锌、铁、银、金等金属和少量矿物杂质)的提纯,并对阳极泥和电解液中金属进行回收和含量测定。请回答以下问题。
①电解时,电解过程中,硫酸铜的浓度会 选填“变大”“不变”或“变小”)。
②电解完成后,该小组同学将电解液过滤后对滤液和阳极泥分别进行处理:
阳极泥的综合利用:稀硝酸处理阳极泥得到硝酸银稀溶液,请你写出该步反应的离子方程式: .
③Cu的回收、滤液成分及含量的测定:以下是该小组设计的一个实验流程。
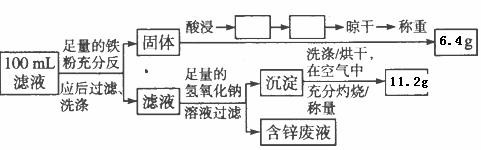
在上述流程中空格内填上相应的操作:过虑 、 ;100 mL滤液中 Fe2+的浓度为 mol/l
查看答案和解析>>
科目:高中化学 来源: 题型:
下列各物质中所含H原子最多的是( )
A.0.1 mol NH4Cl
B.0.1 mol NH4HCO3
C.0.2 mol H2
D.0.2 mol H3PO4
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)等质量的氧气和臭氧的物质的量比为________,所含氧原子的个数比为________。
(2)含相同分子数的CO和CO2,其物质的量之比是________,质量比是________,摩尔质量比是________________________________________,
所含氧原子个数比是________,碳原子个数比是____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
某反应过程中体系的能量变化如图所示,下列说法错误的是( )
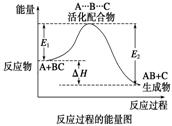
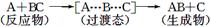
A.反应过程可表示为
B.E1为反应物的平均能量与过渡态的能量差,称为正反应的活化能
C.正反应的热效应为ΔH=E1-E2<0,所以正反应为放热反应
D.此图中逆反应的热效应ΔH=E1-E2<0,所以逆反应为放热反应
查看答案和解析>>
科目:高中化学 来源: 题型:
下列各组的两种物质在溶液中的反应,可用同一离子方程式表示的是
A.Cu(OH)2与盐酸,Cu(OH)2与醋酸
B.BaCl2溶液与Na2SO4溶液,Ba(OH)2溶液与H2SO4溶液
C.NaHCO3溶液与盐酸,Na2CO3溶液与盐酸
D.石灰石与硝酸反应,石灰石与盐酸
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com