
|
向a mL、18 mol·L-1的浓H2SO4中加入足量Cu片,并加热,被还原的H2SO4的物质的量和起酸作用的H2SO4的物质的量分别为 | |
| [ ] | |
A. |
大于9a×10-3 mol,小于18a×10-3 mol |
B. |
等于9a×10-3 mol |
C. |
等于18a×10-3 mol |
D. |
小于9a×10-3 mol |
|
18 mol·L-1的硫酸溶液是浓硫酸,加热条件下可以氧化不活泼的金属铜,表现了浓H2SO4的强氧化性,现有H2SO4物质的量为a×10-3 L×18 mol·L-1=18a×10-3 mol,依化学方程式: Cu+2H2SO4 可知理论上最多只有1/2×18a×10-3 mol的H2SO4被还原(即9a×10-3 mol),但由于硫酸溶液的浓度随反应进行而降低,被还原的H2SO4的物质的量小于9a×10-3 mol,从方程式可知:起氧化剂作用的H2SO4与起酸作用的H2SO4的物质的量相等,起酸作用的H2SO4的量也小于9a×10-3 mol. 解题的关键在于理解硫酸的浓度与其化学性质有关系,随着反应的进行,硫酸的浓度越来越稀,浓硫酸降到一定的浓度时,就不与铜反应了. |


 数学奥赛暑假天天练南京大学出版社系列答案
数学奥赛暑假天天练南京大学出版社系列答案 南大教辅抢先起跑暑假衔接教程南京大学出版社系列答案
南大教辅抢先起跑暑假衔接教程南京大学出版社系列答案科目:高中化学 来源: 题型:
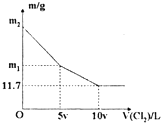 向1OO ml NaBr和NaI的混合溶液中缓慢通入适量的Cl2,充分反应后将所得溶液蒸干,并将所得同体灼烧至恒重,得到m g固体.m与通入Cl2的体积
向1OO ml NaBr和NaI的混合溶液中缓慢通入适量的Cl2,充分反应后将所得溶液蒸干,并将所得同体灼烧至恒重,得到m g固体.m与通入Cl2的体积| A、v=0.224 | B、混合溶液中:c(Na+)=2mol/L | C、m2=25.3 | D、m1=18.55 |
查看答案和解析>>
科目:高中化学 来源: 题型:
(15分).I下表是部分短周期元素的原子半径及主要化合价:
| 元素代号[ | W | R | X | Y | Z | Q | M |
| 原子半径/nm | 0.037 | 0.186 | 0.074 | 0.075 | 0.077 | 0.150 | 0.160 |
| 主要化合价 | +1 | +1 | -2 | -3、+5 | +2、+4 | +3 | +2 |
试用元素符号、化学式回答下列问题:
(1)七种元素中原子半径最大的元素在周期表中位置是 。
M在Z的最高价氧化物中燃烧的化学方程式 。
(2)X可与R按1︰1的原子个数比形成化合物甲,甲中存在的化学键有 ;
X可与W组成含18电子的化合物乙,则乙的电子式为 。
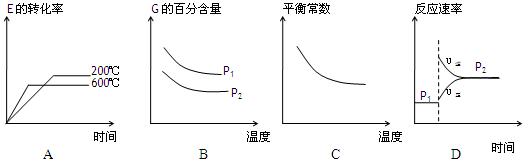
(3)上述元素组成的物质D、E在体积不变的密闭容器中发生可逆反应:2E(g)+D(g)2G(g)根据下表中的数据判断下列图像错误的是 。
|
| p1(MPa) | P2(MPa) |
| 200 | 78.4 | 90.6 |
| 600 | 72.3 | 88.6 |
![]()
II下图为有机物CH3OH新型燃料电池,其中CH3OH由 极(填a或b)通入,写出下列条件下负极电极反应方程式。
(1)若M为氢氧化钾溶液,
(2)若M为熔融的碳酸钾
(3)若M为传递O2-的固体电解质
III一定量的浓硝酸与足量的铁铜合金反应,硝酸被还原
为NO 、 NO2 、 N2O4,其标准状况下的体积均为112mL ,若向所得溶液中加入0.1mol/L的氢氧化钠溶液 mL恰好能使溶液中的金属离子沉淀完全。
查看答案和解析>>
科目:高中化学 来源:2011届山西省高三第四次四校联考(理综)化学部分 题型:填空题
(15分).I下表是部分短周期元素的原子半径及主要化合价:
| 元素代号[ | W | R | X | Y | Z | Q | M |
| 原子半径/nm | 0.037 | 0.186 | 0.074 | 0.075 | 0.077 | 0.150 | 0.160 |
| 主要化合价 | +1 | +1 | -2 | -3、+5 | +2、+4 | +3 | +2 |
 、化学式回答下列问题:
、化学式回答下列问题: 2G(g)根据下表中的数据判断下列图像错误的是 。
2G(g)根据下表中的数据判断下列图像错误的是 。 | p1(MPa) | P2(MPa) |
| 200 | 78.4 | 90.6 |
| 600 | 72.3 | 88.6 |
|
 II下图为有机物CH3OH新型燃料电池,其中CH3OH由 极(填a或b)通入,写出下列条件下负极电极反应方程式。
II下图为有机物CH3OH新型燃料电池,其中CH3OH由 极(填a或b)通入,写出下列条件下负极电极反应方程式。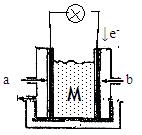
查看答案和解析>>
科目:高中化学 来源:2010-2011学年山西省高三第四次四校联考(理综)化学部分 题型:填空题
(15分).I下表是部分短周期元素的原子半径及主要化合价:
|
元素代号[ |
W |
R |
X |
Y |
Z |
Q |
M |
|
原子半径/nm |
0.037 |
0.186 |
0.074 |
0.075 |
0.077 |
0.150 |
0.160 |
|
主要化合价 |
+1 |
+1 |
-2 |
-3、+5 |
+2、+4 |
+3 |
+2 |
试用元素符号、化学式回答下列问题:
(1)七种元素中原子半径最大的元素在周期表中位置是 。
M在Z的最高价氧化物中燃烧的化学方程式 。
(2)X可与R按1︰1的原子个数比形成化合物甲,甲中存在的化学键有 ;
X可与W组成含18电子的化合物乙,则乙的电子式为 。
(3)上述元素组成的物质D、E在体积不变的密闭容器中发生可逆反应:2E(g)+D(g) 2G(g)根据下表中的数据判断下列图像错误的是
。
2G(g)根据下表中的数据判断下列图像错误的是
。
|
p1(MPa) |
P2(MPa) |
|
|
200 |
78.4 |
90.6 |
|
600 |
72.3 |
88.6 |


II下图为有机物CH3OH新型燃料电池,其中CH3OH由 极(填a或b)通入,写出下列条件下负极电极反应方程式。

(1)若M为氢氧化钾溶液,
(2)若M为熔融的碳酸钾
(3)若M为传递O2-的固体电解质
III一定量的浓硝酸与足量的铁铜合金反应,硝酸被还原
为NO 、 NO2 、 N2O4 ,其标准状况下的体积均为112mL ,若向所得溶液中加入0.1mol/L的氢氧化钠溶液 mL恰好能使溶液中的金属离子沉淀完全。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com