
【题目】为测定某铜和氧化铜的混合物中铜元素的质量分数,某同学设计了如图所示实验装置。
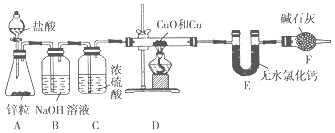
回答下列问题:
(1))装置A中盛装盐酸的仪器的名称为____________。
(2)实验时装置A中可观察到的现象________________________________________ ;发生反应的离子方程式为__________________________________________________。
(3)装置B的作用是_______________________________________________________。
(4)在加热装置D之前,应该进行的一步操作是________________________________,目的是_____________。
【答案】 分液漏斗 锌粒逐渐溶解,有气泡产生 Zn+2H+===Zn2++H2↑ 除去氢气中的HCl 在装置F的出口处收集H2,并检验H2的纯度 确保装置内空气已排尽,以防止加热时发生爆炸
【解析】本题主要考查实验室制取氢气的实验方法。
(1))装置A中盛装盐酸的仪器的名称为分液漏斗。
(2)实验时装置A中可观察到的现象:锌粒逐渐溶解,有气泡产生;发生反应的离子方程式为Zn+2H+===Zn2++H2↑。
(3)盐酸具有挥发性,致使氢气含有氯化氢杂质,装置B的作用是除去氢气中的HCl。
(4)在加热装置D之前,应该进行的一步操作是有气泡产生置F的出口处收集H2,并检验H2的纯度,目的是确保装置内空气已排尽,以防止加热时发生爆炸。


科目:高中化学 来源: 题型:
【题目】常压下羰基化法精炼镍的原理为:Ni(s)+4CO(g)![]() Ni(CO)4(g)。230℃时,该反应的平衡常数K=2×105。已知:Ni(CO)4的沸点为42.2℃,固体杂质不参与反应。
Ni(CO)4(g)。230℃时,该反应的平衡常数K=2×105。已知:Ni(CO)4的沸点为42.2℃,固体杂质不参与反应。
第一阶段:将粗镍与CO反应转化成气态Ni(CO)4;
第二阶段:将第一阶段反应后的气体分离出来,加热至230℃制得高纯镍。
下列判断正确的是
A. 增加c(CO),平衡向正向移动,反应的平衡常数增大
B. 第二阶段,Ni(CO)4分解率较低
C. 第一阶段,在30℃和50℃两者之间选择反应温度,选50℃
D. 该反应达到平衡时,v生成[Ni(CO)4]=4v生成(CO)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】H2S和SO2会对环境和人体健康带来极大的危害,工业上采取多种方法减少这些有害气体的排放,回答下列各方法中的问题。
Ⅰ.H2S的除去
方法1:生物脱H2S的原理为:
H2S+Fe2(SO4)3![]() S↓+2FeSO4+H2SO4
S↓+2FeSO4+H2SO4
4FeSO4+O2+2H2SO4![]() 2Fe2(SO4)3+2H2O
2Fe2(SO4)3+2H2O
(1)硫杆菌存在时,FeSO4被氧化的速率是无菌时的5×105倍,该菌的作用是______________。
(2)由图3和图4判断使用硫杆菌的最佳条件为______________。若反应温度过高,反应速率下降,其原因是______________。

方法2:在一定条件下,用H2O2氧化H2S
(3)随着参加反应的n(H2O2)/n(H2S)变化,氧化产物不同。当n(H2O2)/n(H2S)=4时,氧化产物的分子式为__________。
Ⅱ.SO2的除去
方法1(双碱法):用NaOH吸收SO2,并用CaO使NaOH再生
NaOH溶液![]() Na2SO3
Na2SO3
(4)写出过程①的离子方程式:____________________________;CaO在水中存在如下转化:
CaO(s)+H2O (l) ![]() Ca(OH)2(s)
Ca(OH)2(s)![]() Ca2+(aq)+2OH(aq)
Ca2+(aq)+2OH(aq)
从平衡移动的角度,简述过程②NaOH再生的原理____________________________________。
方法2:用氨水除去SO2
(5)已知25℃,NH3·H2O的Kb=1.8×105,H2SO3的Ka1=1.3×102,Ka2=6.2×108。若氨水的浓度为2.0 mol·L-1,溶液中的c(OH)=_________________mol·L1。将SO2通入该氨水中,当c(OH)降至1.0×107 mol·L1时,溶液中的c(![]() )/c(
)/c(![]() )=___________________。
)=___________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列分子或离子在指定的分散系中能大量共存的一组是( )
A.无色溶液:K+、Cu2+、NO3﹣、AlO2﹣
B.空气: CH4、CO2、SO2、NO
C.氢氧化铁胶体: H+、K+、S2-、Br -
D.各离子物质的量浓度相等的溶液:K+、Mg 2+、SO42-、NO3-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】部分有机物之间的转化关系以及转化过程相对分子质量变化关系如下:
物质转化关系:RCH2OH ![]() RCHO
RCHO![]() RCOOH
RCOOH
相对分子质量:M M2M+14
已知:物质A中只含有C.H、O三种元素,一定条件下能发生银镜反应,物质C的相对分子质量为104.A与其他物质之间的转化关系如图所示:
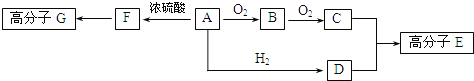
请回答下列问题:
(1)F中含有的官能团有________;G的结构简式___________。
(2)一定条件下B发生银镜反应的化学方程式__________。
(3)由C.D在一定条件下反应还能生成环状化合物,其化学反应方程式为_________。
(4)A的同分异构体很多,写出与A中所含官能团不同,但能与NaOH溶液反应的2种同分异构体的结构简式:_______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】
我国科学家最近成功合成了世界上首个五氮阴离子盐(N5)6(H3O)3(NH4)4Cl(用R代表)。回答下列问题:
(1)氮原子价层电子对的轨道表达式(电子排布图)为_____________。
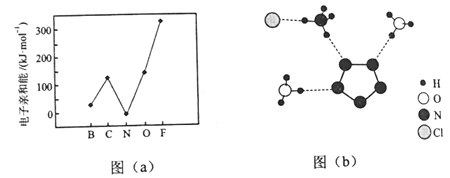
(2)元素的基态气态原子得到一个电子形成气态负一价离子时所放出的能量称作第一电子亲和能(E1)。第二周期部分元素的E1变化趋势如图(a)所示,其中除氮元素外,其他元素的E1自左而右依次增大的原因是___________;氮元素的E1呈现异常的原因是__________。
(3)经X射线衍射测得化合物R的晶体结构,其局部结构如图(b)所示。
①从结构角度分析,R中两种阳离子的相同之处为_________,不同之处为__________。(填标号)
A.中心原子的杂化轨道类型 B.中心原子的价层电子对数
C.立体结构 D.共价键类型
②R中阴离子N5-中的σ键总数为________个。分子中的大π键可用符号![]() 表示,其中m代表参与形成的大π键原子数,n代表参与形成的大π键电子数(如苯分子中的大π键可表示为
表示,其中m代表参与形成的大π键原子数,n代表参与形成的大π键电子数(如苯分子中的大π键可表示为![]() ),则N5-中的大π键应表示为____________。
),则N5-中的大π键应表示为____________。
③图(b)中虚线代表氢键,其表示式为(NH4+)N-H┄Cl、____________、____________。
(4)R的晶体密度为d g·cm-3,其立方晶胞参数为a nm,晶胞中含有y个[(N5)6(H3O)3(NH4)4Cl]单元,该单元的相对质量为M,则y的计算表达式为______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A. 硫酸钠溶液和醋酸铅溶液均能使蛋白质变性
B. 油脂是高级脂肪酸的甘油酯,均不能发生氢化反应
C. H2N—CH2——COOH既能与盐酸反应,又能与氢氧化钠溶液反应
D. 在蛋白质的渗析、盐析、变性过程中都发生了化学变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组离子能够大量共存的是
A. Ag+、NH4+、CO32-、H+ B. Fe3+、H+、SCN-、NO3-
C. Na+、Fe2+、Cl-、NO3- D. H+、MnO4+、Cl-、NO3-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于碱金属单质的叙述正确的是
A. 它们都可以与盐酸反应放出氢气 B. 它们在反应中都被还原
C. 它们都能与氧气反应生成过氧化物 D. 它们都能从FeCl3溶液中置换出Fe
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com