
在铁制品上镀上一定厚度的锌层,以下设计方案正确的是( )
|
| A. | 锌作阳极,镀件作阴极,溶液中含有锌离子 |
|
| B. | 铂作阴极,镀件作阳极,溶液中含有锌离子 |
|
| C. | 铁作阳极,镀件作阴极,溶液中含有亚铁离子 |
|
| D. | 锌用阴极,镀件作阳极,溶液中含有锌离子 |
 寒假创新型自主学习第三学期寒假衔接系列答案
寒假创新型自主学习第三学期寒假衔接系列答案科目:高中化学 来源: 题型:
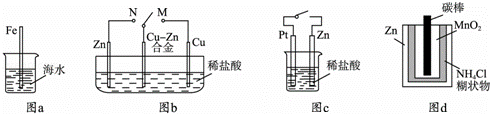
下列与金属腐蚀有关的说法正确的是( )
|
| A. | 图a中,插入海水中的铁棒,越靠近底端腐蚀越严重 |
|
| B. | 图b中,开关由M改置于N时,Cu﹣Zn合金的腐蚀速率减小 |
|
| C. | 图c中,接通开关时Zn腐蚀速率增大,Zn上放出气体的速率也增大 |
|
| D. | 图d中,Zn﹣MnO2干电池自放电腐蚀主要是由MnO2的氧化作用引起的 |
查看答案和解析>>
科目:高中化学 来源: 题型:
离子RO3n﹣中共有x个核外电子,R原子的质量数为A,则R原子核内含中子的数目( )
|
| A. | A+n+48+x | B. | A﹣n﹣24﹣x | C. | A﹣n+24﹣x | D. | A+n+24﹣x |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列叙述正确的是( )
A.还原性:Na>K
B.热稳定性:NaHCO3>Na2CO3
C.等物质的量的NaHCO3和Na2CO3分别跟足量盐酸反应,消耗HCl的物质的量比为1∶2
D.等质量的NaHCO3和Na2CO3分别跟足量盐酸反应,产生CO2的物质的量比为1∶2
查看答案和解析>>
科目:高中化学 来源: 题型:
钠是活泼的碱金属元素,钠及其化合物在生产和生活中有广泛的应用。
完成下列计算:
(1)叠氮化钠(NaN3)受撞击完全分解产生钠和氮气,故可应用于汽车安全气囊。若产生40.32 L(标准状况下)氮气,至少需要叠氮化钠 g。
(2)钠-钾合金可在核反应堆中用作热交换液。5.05 g钠-钾合金溶于200 mL水生成0.075 mol氢气。
①计算溶液中氢氧根离子的物质的量浓度(忽略溶液体积变化)。
②计算并确定该钠-钾合金的化学式。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于化学平衡常数的说法中,正确的是( )
|
| A. | 在任何条件下,化学平衡常数都是一个定值 |
|
| B. | 当改变反应物的浓度时,化学平衡常数会发生改变 |
|
| C. | 化学平衡常数K只与温度、反应物浓度、体系的压强都有关 |
|
| D. | 化学平衡常数K可以推断一个可逆反应进行的程度 |
查看答案和解析>>
科目:高中化学 来源: 题型:
0.3moL气态高能燃料乙硼烷(B2H6)在氧气中燃烧,生成固态B2O3和液态水,放出649.5KJ热量,请写出乙硼烷燃烧的热化学方程式 ;又已知:H2O(l)→H2O(g);△H=+44kJ/moL,则11.2L(标准状况)乙硼烷完全燃烧生成气态水时放出的热量是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
NA为阿伏加德罗常数,下列叙述正确的是( )
|
| A. | 标准状况下,含NA个氩原子的氩气的体积约为11.2 L |
|
| B. | 31g白磷分子中,含有的共价单键数目是NA个 |
|
| C. | 6 g金刚石晶体中含有的碳碳键数目为2×6.02×1023 |
|
| D. | 4.5 g SiO2晶体中含有的硅氧键数目为0.3×6.02×1023 |
查看答案和解析>>
科目:高中化学 来源: 题型:
写出下列反应的离子方程式或化学方程式
(1)Ba(OH)2与H2SO4反应:(离子方程式) ;
(2)Fe与HCl反应:(离子方程式) ;
(3)Al与HCl溶液反应:(化学方程式) .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com