
某化学兴趣小组的同学学习了同周期元素性质递变规律后,设计了一套实验方案进行实验探究,并记录了有关实验现象如下表:
| 实验操作 | 实验现象 |
| Ⅰ.用砂纸打磨后的镁带与沸水反应,再向反应后溶液中滴加酚酞 Ⅱ.向新制的H2S饱和溶液中滴加新制的氯水 Ⅲ.钠与滴有酚酞溶液的冷水反应 Ⅳ.镁带与2 mol·L-1的盐酸反应 Ⅴ.铝条与2 mol·L-1的盐酸反应 Ⅵ.向AlCl3溶液滴加NaOH溶液至过量 | A.浮于水面,熔成一个小球,在水面上无定向 移动,随之消失,溶液变红色 B.产生气体,可在空气中燃烧,溶液变成浅红 色 C.反应不十分强烈,产生的气体可以在空气中 燃烧 D.剧烈反应,产生可燃性气体 E.生成白色胶状沉淀,进而沉淀消失 F.生成淡黄色沉淀 |
请你帮助该同学整理并完成实验报告
(1)实验目的:___________________________________________________。
(2)实验用品:仪器①______________、②____________、③____________、④试管夹、⑤镊子、⑥小刀、⑦玻璃片、⑧砂纸、⑨胶头滴管等。
药品:钠、镁带、铝条、2 mol·L-1的盐酸、新制的氯水、新制的饱和H2S溶液、AlCl3溶液、NaOH溶液等。
(3)请你写出上述的实验操作与对应的现象
Ⅰ________、Ⅱ________、Ⅲ________、Ⅳ________、Ⅴ________、Ⅵ________。(用A~F表示)
写出实验操作Ⅱ、Ⅵ的离子反应方程式
实验Ⅱ________________________________________________________________________;
实验Ⅵ________________________________________________________________________。
(4)实验结论:___________________________________________________。
 智能训练练测考系列答案
智能训练练测考系列答案科目:高中化学 来源: 题型:
下图为CaF2、H3BO3(层状结构,层内的H3BO3分子通过氢键结合)、金属铜三种晶体的结构示意图,请回答下列问题:
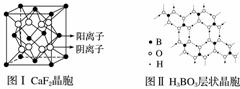
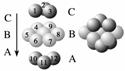
图Ⅲ 铜晶体中铜原子堆积模型
(1)图Ⅰ所示的CaF2晶体中与Ca2+最近且等距离的F-数为________________,图Ⅲ中未标号的铜原子形成晶体后周围最紧邻的铜原子数为________________________________________________________________________。
(2)图Ⅱ所示的物质结构中最外能层已达8电子结构的原子是________,H3BO3 晶体中B原子个数与极性键个数比为____________。
(3)金属铜具有很好的延展性、导电性、传热性,对此现象最简单的解释是用________理论。
(4)三种晶体中熔点最低的是________(填化学式),其晶体受热熔化时,克服的微粒之间的相互作用为________________________________________________________________________
________________________________________________________________________。
(5)已知两个距离最近的Ca2+核间距离为a×10-8cm,结合CaF2晶体的晶胞示意图,CaF2晶体的密度为________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列与有机物的结构、性质有关的叙述正确的是( )
A.苯、油脂均不能使酸性KMnO4溶液褪色
B.医用酒精的浓度通常为95%
C.乙醇可以被氧化为乙酸,二者都能发生取代反应
D.淀粉和蛋白质均可作为生产葡萄糖的原料
查看答案和解析>>
科目:高中化学 来源: 题型:
在水中加入等物质的量的Ag+、Pb2+、Na+、SO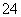 、NO
、NO 、Cl-,该溶液放在用惰性电极材料作电极的电解槽中,通电片刻,则氧化产物与还原产物质量比为( )
、Cl-,该溶液放在用惰性电极材料作电极的电解槽中,通电片刻,则氧化产物与还原产物质量比为( )
A.35.5∶108 B.16∶207
C.8∶1 D.108∶35.5
查看答案和解析>>
科目:高中化学 来源: 题型:
通过化学反应原理猜测可能生成哪些物质,对这些物质逐一进行检验来确定究竟含有哪些物质。正确解答此类试题的关键:(1)猜测要全面;(2)熟记常见物质的检验方法。
| [典例] | 审题指导 |
| 某研究性学习小组用下列装置(铁架台等夹持仪器略)探究氧化铁与乙醇的反应,并检验反应产物。 | 联想:乙醇的催化氧化。 |
| (1)用2%的CuSO4溶液和10%的NaOH溶液配制Cu(OH)2悬浊液的注意事项是________________________________________________________________________。 | 新制Cu(OH)2悬浊液与醛基的反应需要碱性条件。 |
| (2)为快速得到乙醇气体,可采用的方法是________________________________________________________________________。 若实验时小试管中的溶液已经开始发生倒吸,可采取的措施是________(填字母)。 a.取下小试管 b.移去酒精 c.将导管从乳胶管中取下 d.以上都可以 | ①升高温度可加速乙醇的挥发。 ②若液体倒吸入加热的反应管,可能会造成反应管炸裂,取下小试管已无济于事,因“溶 液已经开始发生倒吸”。 |
| (3)如图实验,观察到红色的Fe2O3全部变为黑色固体M,充分反应后停止加热。取下小试 管,加热,有砖红色沉淀生成。 为了检验M的组成,进行下列实验。 ①M能被磁铁吸引;加入足量稀硫酸,振荡,固体全部溶解,未观察到有气体生成; ②经检验溶液中有铁离子和亚铁离子,检验铁离子的方法是_____________________;证明溶液含有亚铁离子的方法是________________________________________________________________________。 能得出的结论是________(填字母)。 a.M中一定有+3价和+2价铁,不能确定是否有0价铁 b.M中一定有+3价和0价铁,无+2价铁 c.M中一定有+3价铁,0价和+2价铁至少有一种 d.M中一定有+3价、+2价和0价铁 | 破题关键 分析黑色固体(M)可能的成分,铁的氧化物Fe3O4、FeO和铁粉均为黑色,Fe3O4中既有+3价铁又有+2价铁,且具有磁性,Fe3+能溶 解单质铁。 易错警示 已知溶液中有Fe3+,检验Fe2+不能用KSCN 溶液。 |
| (4)若M的成分可表达为FexOy,用CO还原法定量测定其化学组成。称取m g M样品进行定量测定,实验装置和步骤如下:
①组装仪器;②点燃酒精灯;③加入试剂;④打开分液漏斗活塞;⑤检查气密性;⑥停止加热;⑦关闭分液漏斗活塞;⑧…… 正确的操作顺序是________(填字母)。 a.①⑤④③②⑥⑦⑧ b.①⑤③④②⑥⑦⑧ c.①③⑤④②⑦⑥⑧ d.①③⑤②④⑥⑦⑧ 若M完全被还原后碱石灰增重n g,则 | 破题关键 Ⅰ.检查气密性属于实验的准备阶段,应在加药品前进行。 Ⅱ.类比氢气还原氧化铜。 Ⅲ.碱石灰增加的质量即为反应产生的CO2的质量,得关系式M中n(O)=n(CO2)。 |
查看答案和解析>>
科目:高中化学 来源: 题型:
SO2是一种大气污染物,某兴趣小组欲探究SO2的性质及绿色实验方法,设计如下方案:
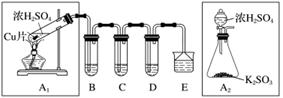
(1)B、C、D分别用于检验SO2的漂白性、还原性和氧化性。其中C、D分别为碘水和硫化氢的水溶液,则B中所盛试剂为__________,C中反应的离子方程式为________________________________________________________________________。
(2)为了实现绿色实验的目标,某同学重新设计了如上右图A2的制取装置来代替A1装置,与A1装置相比,A2装置的优点是____________________________________________________
(任写一点即可)。
(3)E中用氨水吸收尾气中的SO2,“吸收液”中可能含有OH-、SO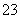 、SO
、SO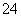 、HSO
、HSO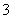 等阴离子。已知亚硫酸氢盐一般易溶于水,SO2也易溶于水。现有仪器和试剂为小烧杯、试管、玻璃棒、胶头滴管、过滤装置和滤纸;2 mol·L-1盐酸、2 mol·L-1 HNO3、1 mol·L-1 BaCl2溶液、1 mol·L-1 Ba(OH)2溶液、品红溶液、蒸馏水。请设计实验证明“吸收液”中存在SO
等阴离子。已知亚硫酸氢盐一般易溶于水,SO2也易溶于水。现有仪器和试剂为小烧杯、试管、玻璃棒、胶头滴管、过滤装置和滤纸;2 mol·L-1盐酸、2 mol·L-1 HNO3、1 mol·L-1 BaCl2溶液、1 mol·L-1 Ba(OH)2溶液、品红溶液、蒸馏水。请设计实验证明“吸收液”中存在SO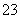 和HSO
和HSO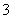 ,完成下表的实验操作、预期现象和结论:
,完成下表的实验操作、预期现象和结论:
| 实验操作 | 预期现象与结论 |
| 步骤1:取适量“吸收液”于小烧杯中,用胶头滴管取1 mol·L-1 BaCl2溶液滴入小烧杯中直至过量 | 若出现白色浑浊,则溶液中存在SO |
| 步骤2:将小烧杯中的浊液过滤、洗涤,再用适量水把附在滤纸上的固体冲入另一小烧杯中;向冲下的固体______________ | |
| 步骤3: |
查看答案和解析>>
科目:高中化学 来源: 题型:
分析下图所示的四个原电池装置,其中结论正确的是( )
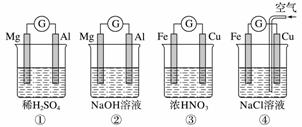
A.①②中Mg作负极,③④中Fe作负极
B.②中Mg作正极,电极反应式为6H2O+6e-===6OH-+3H2↑
C.③中Fe作负极,电极反应式为Fe-2e-===Fe2+
D.④中Cu作正极,电极反应式为2H++2e-===H2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
下列方程式①AgCl(s)Ag+(aq)+Cl-(aq)、
②AgCl===Ag++Cl-、 ③CH3COOHCH3COO-+H+各表示什么意义?
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com