
科目:高中化学 来源: 题型:选择题
| A. | 向平衡体系中加入少量KCl固体或Fe(SCN)3固体,溶液红色都变浅 | |
| B. | 向平衡体系中加入少量FeCl3固体或KSCN固体,溶液红色加深 | |
| C. | 向平衡体系中加入水稀释,平衡不移动,但溶液红色变浅 | |
| D. | 该反应的离子方程式为:3KSCN+Fe3+═Fe(SCN)3(血红色)+3K+ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
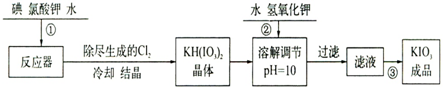
| 温度/℃ | 20 | 40 | 60 | 80 |
| KIO3g/100g水 | 8.08 | 12.6 | 18.3 | 244.8 |
| 操作步骤 | 实验现象 |
| 取1g纯净的NaCl,甲3mL水配制溶液 | 溶液无变化 |
| 滴入5滴淀粉溶液和1mL0.1mol.L-1KI溶液,振荡 | 溶液无变化 |
| 然后再滴入1滴1mol.L-1的H2SO4,从发振荡 | 溶液变蓝色 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 加入蒸馏水 | B. | 加热 | C. | 加入NaHSO4固体 | D. | 加入浓盐酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 在密闭容器中,对于可逆反应A+3B?2C(g),平衡时C的体积分数与温度和压强的关系如图所示,下列判断正确的是( )
在密闭容器中,对于可逆反应A+3B?2C(g),平衡时C的体积分数与温度和压强的关系如图所示,下列判断正确的是( )| A. | 若正反应方向△H<0,则T1>T2 | |
| B. | 压强增大时,混合气体的平均相对分子质量减小 | |
| C. | B一定为气体 | |
| D. | A一定为气体 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 微量元素虽然含量占人体的0.01以下,但对于维持生命活动,促进健康和发育却有极其重要的作用 | |
| B. | 钙元素属于微量元素 | |
| C. | 青少年或成人缺碘可引起甲状腺肿大 | |
| D. | 摄入的铁越多越利于身体健康 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 某物质的溶液中由水电离出的c(H+)=1×10-amol/L,若a>7时,则该溶液的pH一定为14-a | |
| B. | 某溶液中存在的离子有S2-、HS-、OH-、Na+、H+,则离子浓度一定是c(Na+)>c(S2-)>c(OH-)>c(HS-)>c(H+) | |
| C. | 将0.2 mol/L的某一元酸HA溶液和0.1mol/L NaOH溶液等体积混合后溶液pH大于7,则反应后的混合液:2c(OH-)=2c(H+)+c(HA)-c(A-) | |
| D. | ①Na2CO3溶液②CH3COONa溶液③NaOH溶液,若3种溶液pH均为9,则它们物质的量浓度大小顺序是①>②>③ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 长期饮用蒸馏水对身体有益 | B. | 电解水时,正极产生的气体是氢气 | ||
| C. | 利用蒸馏方法可以淡化海水 | D. | 水直接由氢原子和氧原子构成 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com