
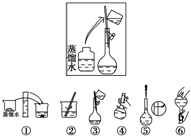
 某同学帮助水质检测站配制500mL 0.5mol•L-1NaOH溶液以备使用.其操作步骤如图所示,则方框中操作的位置为( )
某同学帮助水质检测站配制500mL 0.5mol•L-1NaOH溶液以备使用.其操作步骤如图所示,则方框中操作的位置为( )| A. | ①与②之间 | B. | ②与③之间 | C. | ④与⑤之间 | D. | ⑤与⑥之间 |
分析 配制一定物质的量浓度的溶液的操作步骤:计算、称量、溶解、冷却、移液、洗涤、定容、摇匀等操作,如图所示的操作为移液洗涤后向容量瓶内加水,应在加水振荡与定容之间.
解答 解:配制500mL 0.5mol•L-1NaOH溶液的操作步骤:首先计算出需要的药品的质量,然后用托盘天平称量,后放入烧杯中溶解,同时用玻璃棒搅拌,待溶液冷却至室温后,用玻璃杯引流移液至500ml容量瓶,然后洗涤烧杯和玻璃棒2至3次,将洗涤液也注入容量瓶,然后向容量瓶中注水,至液面离刻度线1~2cm时,改用胶头滴管逐滴加入,至凹液面与刻度线相切,然后摇匀、装瓶.图所示的步骤是移液洗涤后向容量瓶内加水,应在加水振荡与定容之间,故应在④和⑤之间,
故选C.
点评 本题考查了一定物质的量浓度溶液的配制以及误差分析,难度不大,注意实验的基本操作方法和注意事项.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:选择题
| A. | 配制100mL 1.0mol/LCuSO4溶液:将25g CuSO4•5H2O溶于100mL蒸馏水中 | |
| B. | 配制6mol/L100mL硫酸时,定容后应将容量瓶沿顺时针方向摇匀 | |
| C. | 盛放NaOH溶液时,使用带玻璃塞的磨口瓶 | |
| D. | 可以采用溶解、蒸发浓缩、冷却结晶、过滤的方法分离NaCl和KNO3固体混合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 溶解平衡的本质是结晶速率等于溶解速率 | |
| B. | 在不饱和溶液中,溶质的溶解速率小于结晶速率 | |
| C. | 在饱和溶液中,晶体的质量不改变,形状可能改变 | |
| D. | 当物质达到溶解平衡时,不改变外界条件,溶液的浓度也不改变 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
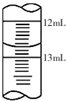 酱油是一种常用调味剂,根据国标要求酱油中NaCl的含量不应低于15g/100mL.莫尔法是较简单的一种测量Cl-含量的方法.现采用该法测量某市售酱油是否符合NaCl含量标准要求.实验原理如下(25℃):
酱油是一种常用调味剂,根据国标要求酱油中NaCl的含量不应低于15g/100mL.莫尔法是较简单的一种测量Cl-含量的方法.现采用该法测量某市售酱油是否符合NaCl含量标准要求.实验原理如下(25℃):查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 25℃时,由水电离出的c(H+)=1×10-12 mol•L-1的溶液中:Na+、NH4+、I-、NO3- | |
| B. | 能使酚酞变红的溶液中:K+、Na+、Cl-、CO32- | |
| C. | NaHCO3溶液中:K+、Na+、SO42-、Al3+ | |
| D. | 常温下,c(H+)/c(OH-)=1×1012的溶液中:Fe2+、Mg2+、Cl-、NO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 石墨比金刚石稳定 | B. | 金刚石比石墨稳定 | ||
| C. | 石墨转化为金刚石是一个物理变化 | D. | 石墨和金刚石是同一种物质 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
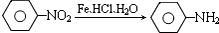 (苯胺、弱碱性、易被氧化)
(苯胺、弱碱性、易被氧化)
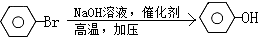


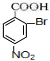 D:
D: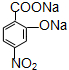 ;
;查看答案和解析>>
科目:高中化学 来源: 题型:解答题
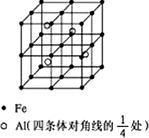 第四周期过渡元素Fe、Ti可与C、H、N、O形成多种化合物.
第四周期过渡元素Fe、Ti可与C、H、N、O形成多种化合物.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 新制氯水中没有氯气分子 | |
| B. | 新制氯水在光照的条件下,可以产生气体,该气体是氯气 | |
| C. | 新制氯水中滴加硝酸银溶液,没有任何现象 | |
| D. | 新制氯水可以使干燥的布条褪色 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com