
【题目】高血脂严重影响人体健康,化合物E是一种临床治疗高血脂症的药物。E的合成路线如下(部分反应条件和试剂略):

已知:
请回答下列问题:
(1)试剂II中官能团的名称是______________,第②步的反应类型是_______,E 的分子式是_______,E分子中共平面的碳原子数最多是_______个。
(2)第①步反应的化学方程式是______________。
(3)试剂II与足量NaOH溶液共热后的产物F的名称是_________, F经催化氧化后可发生银镜反应,该银镜反应的化学方程式为______________。
(4)第⑥步反应的化学方程式是______________。
(5)第⑦步反应中,试剂III为单碘代烷烃,其结构简式是______________。
(6)C的同分异构体H在酸性条件下水解,生成X、Y和CH3(CH2)4OH 。若X含有羧基和苯环,且X和Y的核磁共振氢谱都只有两种类型的吸收峰,则H的结构简式为____________, X与Y发生缩聚反应所得缩聚物的结构简式是____________。
【答案】 溴原子 取代反应 C15H22O2 13 CH3CH(COOH)2+2CH3OH![]() CH3CH(COOCH3)2+ 2H2O 1,3丙二醇 OHCCH2CHO+4Ag(NH3)2OH
CH3CH(COOCH3)2+ 2H2O 1,3丙二醇 OHCCH2CHO+4Ag(NH3)2OH![]() H4NOOCCH2COONH4+4Ag↓+6NH3+2H2O
H4NOOCCH2COONH4+4Ag↓+6NH3+2H2O 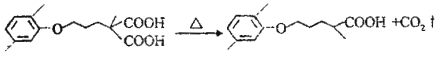 CH3I
CH3I ![]()
![]()
【解析】(1)试剂Ⅱ的结构简式为BrCH2CH2CH2Br,含有的官能团为溴原子;对比![]() 、
、![]() 、BrCH2CH2CH2Br的结构可知,反应②属于取代反应;
、BrCH2CH2CH2Br的结构可知,反应②属于取代反应;![]() 的分子式是C15H22O2,结合苯环的平面结构特征,其分子中共平面的碳原子数最多是13个。
的分子式是C15H22O2,结合苯环的平面结构特征,其分子中共平面的碳原子数最多是13个。
(2)反应①是CH3CH(COOH)2与CH3OH发生酯化反应生成CH3CH(COOCH3)2,反应方程式为:CH3CH(COOH)2+2CH3OH![]() CH3CH(COOCH3)2+2H2O;
CH3CH(COOCH3)2+2H2O;
(3)试剂II与足量NaOH溶液共热后的产物F为HOCH2CH2CH2OH,其名称是1,3丙二醇,F经催化氧化后生成的OHCCH2CHO可发生银镜反应,该银镜反应的化学方程式为OHCCH2CHO+4Ag(NH3)2OH![]() H4NOOCCH2COONH4+4Ag↓+6NH3+2H2O;
H4NOOCCH2COONH4+4Ag↓+6NH3+2H2O;
(4)反应④在碱性条件下发生酯的水解反应生成B,B酸化生成C,则C为![]() ,结合信息可知D
,结合信息可知D![]() ,第⑥步反应的化学方程式是:
,第⑥步反应的化学方程式是:![]()
![]()
![]() +CO2↑;
+CO2↑;
(5)第⑦步反应中,试剂Ⅲ为单碘代烷烃,对比D、E的结构简式可知试剂Ⅲ为CH3I;
(6)C的分子式为C15H20O5,其同分异构体在酸性条件下水解,说明含有酯基,生成X、Y和CH3(CH2)4OH,生成物X含有羧基和苯环,且X和Y的核磁共振氢谱均只有两种类型的吸收峰,则X为![]() ,Y为HOCH2CH2OH,则H的结构简式为
,Y为HOCH2CH2OH,则H的结构简式为![]() ;X和Y发生缩聚反应所得缩聚物的结构简式是:
;X和Y发生缩聚反应所得缩聚物的结构简式是:![]() ,
,


科目:高中化学 来源: 题型:
【题目】已知:2H2S(g)+O2(g)===S2(s)+2H2O(l) ΔH=-632 kJ·mol-1。下图为H2S燃料电池的示意图。下列说法正确的是
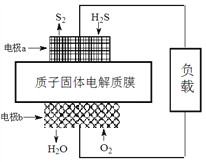
A. 电极a为电池的负极
B. 电极b上发生的电极反应为:O2+2H2O+4e-===4OH-
C. 每有1mol氧气参加反应,电池内部吸收632 kJ热能
D. 每34 g H2S参与反应,电路中有2 mol 电子通过
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的数值,下列说法正确的是( )
A. 常温常压下,56 g乙烯和丙烯的混合气中含有的碳原子数为4NA
B. 1.2 g NaHSO4晶体中含有的阳离子和阴离子的总数为0.03NA
C. 12 g金刚石中含有的共价键数为4NA
D. 1 mol Fe2+与足量的H2O2溶液反应,转移2NA个电子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铁是生产生活中应用最广泛的金属,炼铁技术备受关注,己知:
①2Fe2O3(s)+3C(s)![]() 4Fe(s)+3CO2(g) △H=+460.5kJ/mol
4Fe(s)+3CO2(g) △H=+460.5kJ/mol
②Fe2O3(s)+3CO(g)![]() 2Fe(s)+3CO2(g) △H=-28.5kJ/mol
2Fe(s)+3CO2(g) △H=-28.5kJ/mol
③ 断裂lmol CO(s)气体中的化学键需要吸收1O76kJ的能量
断裂lmolCO2(s)气体中的化学键需要吸收1490kJ的能量
请回答下列问题:
(l)断裂1molC(s)中所有化学键需要吸收的能量为_________。
(2)T1℃时,向密闭容器中加入一定量的Fe2O3和C,发生反应①,达到平衡后,CO2的浓度为a mol/L;其他条件不变,缩小容器容积,再次达到平衡时,CO2的浓度为bmol/L,则a____b (选填“>”“<”或“=”)。
(3)起始温度均为T2℃时,向容积为10L的三个恒容密闭容器中,分别加入一定量的Fe2O3和CO发生反应②,测得相关数据如表所示:
编号 | 容器 | 起始时物质的量/mol | 平衡时物质的量/mol | 平衡常数(K) | |
Fe2O3 | CO | Fe | |||
1 | 恒温 | 0.5 | 1.5 | 0.8 | K1 |
2 | 恒温 | 2 | 3 | m | K2 |
3 | 绝热 | 1 | 1.5 | n | K3 |
①T2℃时,容器1中反应的平衡常数Kl=_______。
②容器2中,5min达到平衡,则0~5min内以CO2表示该反应的速率v(CO2)=_____。
③对于三个容器中的反应,下列说法正确的是(填选项字母)________。
A.m>2n B. 容器1和容器2中CO的平衡转化率al<a2
C. K1=K3 D. 平衡时气体压强:P3>Pl
(4)T2℃时,向恒压密闭容器中充入0.5molFe2O3和1.0molCO,发生反应② ,CO和CO2的物质的量浓度(c)与时间(t)的关系如图所示。

6min时,改变的外界条件为_________,理由为___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中正确的是
A. 同一原子中,1s、2s、3s电子的能量逐渐减小
B. 3p2表示3p能级有两个轨道
C. 处于最低能量状态的原子叫做基态原子
D. 同一原子中,2p、3p、4p能级的轨道数依次增多
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列除杂或提纯的操作方法不正确的是
A. 镁粉中含少量铝粉:加足量氢氧化钠溶液充分搅拌后过滤
B. 碳酸钠溶液中含少量碳酸氢钠:加足量澄清石灰水
C. 自来水中含少量Fe2+:蒸馏
D. 硝酸钾固体中含少量氯化钾:配制80℃的饱和溶液,冷却结晶、过滤、洗涤、干燥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】SO2是重要的化工原料,但其造成的环境问题也引起了人们的关注。开发寻找SO2的合理替代品是目前化工行业的新动态。
(1)SO2可以与水反应,反应的化学方程式为____________________________________。SO2是大气的主要污染物,是造成__________________的根源。
(2)工业上常用黄铁矿(FeS2)制备SO2,黄铁矿中S的化合价为____________。黄铁矿煅烧后生成1.6gFe2O3,转移的电子数为________。
(3)工业上使用碱液吸收SO2,使排放的尾气达到合格标准:
①将标准状况下11.2LSO2通入到2L0.5mol·L-1的氨水中,所得溶液中溶质是_________(填化学式)。
②常温下,若用1LNaOH若用吸收0.01molSO2,完全吸收后溶液中c(Na+)=c(SO32-)+c(HSO3-)+c(H2SO3),则原NaOH溶液的pH值为________。
(4)连二亚硫酸钠(Na2S2O4)与SO2相似,具有极强的还原性,可用于保存水果食物。现可用如图所示方法通过吸收SO2和NO,获得Na2S2O4和NH4NO3(Ge为铈元素)

①装置II中,酸性条件下,NO被Ge4+氧化的产物主要是NO3-、NO2-,请写出生成等物质的量的NO3-和NO2-的离子方程式:_______________________________。
②装置III的作用之一是用质子交换膜电解槽电解使得Ge4+再生,同时在另一极生成S2O42-的电极反应式为___________________________。
(5)现今,科学家已研发出比SO2更安全的偏重亚硫酸盐(K2S2O5),工业上常用2KHSO3=K2S2O5+H2O的方法制备。我国要求红酒中添加K2S2O5的标准(按等硫元素质量的SO2计)为0.25g/L。今酿造500吨葡萄酒,需加入K2S2O5的质量为_______。(葡萄酒的密度近似为水,计算结果保留小数点后2位)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于硅及化合物的性质、用途有关叙述中,不正确的是( )
A. 晶体硅是良好的半导体材料B. 硅单质可用来制造太阳能电池
C. 二氧化硅是光导纤维材料D. 常温下二氧化硅不能与NaOH溶液反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com