
【题目】A、B、C、D、E、F六种元素,原子序数依次增大,A是周期表中原子半径最小的元素,B原子的最外层上有4个电子;D的阴离子和E的阳离子具有相同的电子层结构,两元素的单质反应,生成一种淡黄色的固体,F的L层电子数等于K、M两个电子层上的电子数之和。(用元素符号或化学式填空回答以下问题)
(1)B为________,D为________,E为________。
(2)C元素在周期表中的位置________。
(3)B、D两元素形成化合物属(“离子”或“共价”)化合物________。
(4)F原子结构示意图为________。
(5)写出BD2和E2D2的电子式:_______;_______。
(6)B、C、D的最简单氢化物稳定性由强到弱依次为:______。(填化学式)
(7)写出F元素的最高价氧化物的水化物和B反应的化学方程式:________。
(8)E与F两元素可形成化合物,用电子式表示其化合物的形成过程:_________。
【答案】C O Na 第二周期第ⅤA族 共价 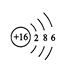
![]()
![]() H2O>NH3>CH4 C+2H2SO4
H2O>NH3>CH4 C+2H2SO4![]() CO2↑+2SO2↑+2H2O
CO2↑+2SO2↑+2H2O ![]()
【解析】
短周期A、B、C、D、E、F六种元素,原子序数依次增大,A的原子半径最小,则A为H元素;F的L层电子数等于K、M两个电子层上的电子数之和,L层上有8个电子,K层上有2个电子,则M层上有6个电子,则F为S元素;D的阴离子和E的阳离子具有相同的电子层结构,两元素的单质反应,生成一种淡黄色的固体,该固体为过氧化钠,则D为O元素、E为Na元素;B原子的最外层上有4个电子,原子序数小于O,则B为C元素,则C为N元素,据此结合元素周期律分析解答。
(1)根据分析可知,A为H元素、B为C元素、C为N元素,D为O元素、E为Na元素、F为S元素,故答案为:C;O;Na;
(2)C为N元素,原子序数为7,位于周期表中第二周期第ⅤA族,故答案为:第二周期第ⅤA族;
(3)B、D两元素形成化合物为一氧化碳或二氧化碳,均属于共价化合物,故答案为:共价;
(4)F为S元素,原子结构示意图为![]() ,故答案为:
,故答案为:![]() ;
;
(5)BD2为二氧化碳,属于共价化合物,电子式为![]() ;E2D2为过氧化钠,为离子化合物,电子式为
;E2D2为过氧化钠,为离子化合物,电子式为![]() ,故答案为:
,故答案为:![]() ;
;![]() ;
;
(6)元素的非金属性越强,最简单氢化物稳定性越强,B、C、D的最简单氢化物稳定性由强到弱依次为H2O>NH3>CH4,故答案为:H2O>NH3>CH4;
(7)F元素的最高价氧化物的水化物为H2SO4,浓硫酸和C反应的化学方程式为C+2H2SO4![]() CO2↑+2SO2↑+2H2O,故答案为:C+2H2SO4
CO2↑+2SO2↑+2H2O,故答案为:C+2H2SO4![]() CO2↑+2SO2↑+2H2O;
CO2↑+2SO2↑+2H2O;
(8)E与F两元素形成的化合物为Na2S,用电子式表示其化合物的形成过程为![]() ,故答案为:
,故答案为:![]()


科目:高中化学 来源: 题型:
【题目】在恒温恒压下,向密闭容器中充入4molSO2和2molO2,发生如下反应:2SO2(g)+O2(g) ![]() 2SO3(g) ΔH<0。2min后,反应达到平衡,生成SO3为1.4mol,同时放出热量QkJ,则下列分析正确的是
2SO3(g) ΔH<0。2min后,反应达到平衡,生成SO3为1.4mol,同时放出热量QkJ,则下列分析正确的是
A. 在该条件下,反应前后的压强之比为6∶5.3
B. 若把“恒温恒压下”改为“恒压绝热条件下”反应,平衡后n(SO3)>1.4mol
C. 若反应开始时容器容积为2L,则v(SO3)=0.35mol·L-1·min-1
D. 若把“恒温恒压下”改为“恒温恒容下”反应,达平衡时放出热量小于Q kJ
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期元素W、X、Y、Z的原子序数依次递增,a、b、c、d、e、f是由这些元素成的化合物,d是淡黄色粉末,m为元素Y的单质,通常为无色无味的气体。上述物质的转化关系如图所示。下列说法错误的是

A. 简单离子半径:Z<Y
B. d中既含有离子键又含有共价键, 其中阳离子和阴离子的数目之比为2:1
C. 简单气态氢化物的热稳定性:Y>X
D. 由上述4种元素组成的化合物的水溶液一定显酸性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用CO和H2合成甲醇,其反应的化学方程式为CO(g)+2H2(g)CH3OH(g).今在一容积可变的密闭容器中,充有10mol CO和20mol H2用于合成甲醇.CO的平衡转化率(α)与温度(T)、压强(P)的关系如图所示:

(1)写出该反应的平衡常数表达式为__________________.
(2)上述合成甲醇的反应为________反应(填“放热”或“吸热”). A、B、C三点的平衡常数KA、KB、KC的大小关系为____________.A、B两点对应的压强大小关系是PA________PB(填“大于”、“小于”或“等于”).
(3)若反应达到平衡状态A时,保持容器体积及体系温度不变,再向容器中充入2mol CO(g)、4molH2(g)、 2molCH3OH(g)则平衡向______方向移动(填“正”或“逆”)
(4)通常状况下取一定量的甲醇充分完全燃烧生成27克的水,放出热量544.35KJ,请写出表示甲醇燃烧热的热化学反应方程式_______________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(I)用锌片、铜片连接后浸入稀硫酸溶液中,构成了原电池,工作一段时间,锌片的质量减少了3.25克,铜表面析出了氢气________L(标准状况下)。导线中通过_______mol电子。
(II)选择适宜的材料和试剂设计一个原电池,以便完成下列反应。
Cu+2AgNO3===2Ag+Cu(NO3)2
(1)请指出正极材料、负极材料、电解质溶液(写化学式):
正极:______,负极:_____,电解质溶液:______。
(2)写出电极反应式:正极:___________,负极:___________。
(3)溶液中Ag+向______极移动,电子从______极流向_____极。(填“正”或“负”)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com