
| A. | BeCl2 | B. | H2O | C. | HCHO | D. | CS2 |
分析 根据价层电子对互斥理论确定分子的空间构型及原子杂化方式,价层电子对个数=σ键个数+孤电子对个数,据此分析解答.
解答 解:A.BeCl2分子中,铍原子含有两个共价单键,不含孤电子对,所以价层电子对数是2,中心原子以sp杂化轨道成键,分子的立体构型为直线形,故A错误;
B.水分子中孤电子对数=$\frac{6-2×1}{2}$=2,水分子氧原子含有2个共价单键,所以价层电子对数是4,中心原子以sp3杂化轨道成键,价层电子对互斥模型为四面体型,含有2对孤对电子,分子的立体构型为V形,故B正确;
C.HCHO分子内(H2C=O)碳原子形成3个σ键,无孤对电子,分子中价层电子对个数=3+0=3,杂化方式为sp2杂化,价层电子对互斥模型为平面三角形,没有孤电子对,分子的立体构型为平面三角形,故C错误;
D.二硫化碳分子中碳原子含有2个σ键且不含孤电子对,采用sp杂化,其空间构型是直线形,故D错误;
故选B.
点评 本题考查了微粒空间构型及原子杂化方式,根据价层电子对互斥理论来分析解答,难点的孤电子对个数的计算方法,为常考查点,要熟练掌握,题目难度中等.


科目:高中化学 来源: 题型:解答题
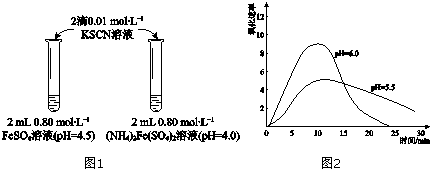
| 物质 | 0min | 1min | 1h | 5h |
| FeSO4 | 淡黄色 | 桔红色 | 红色 | 深红色 |
| (NH4)2Fe(SO4)2 | 几乎无色 | 淡黄色 | 黄色 | 桔红色 |
| 操作 | 现象 |
| 取取2mLpH=4.0的0.80mol•L-1FeSO4溶液,加加2滴0.01mol•L-1KSCN溶液,观察. | 与实验Ⅰ中(NH4)2Fe(SO4)2溶液现象相同. |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②⑤ | B. | ③④⑤ | C. | ③⑤⑥ | D. | ②④⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 ;
;查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH3COONH4、H2O、水晶 | B. | H2SO4、硫磺、石墨 | ||
| C. | KOH、SO3、Ar | D. | Ba(OH)2、玻璃、金刚石 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
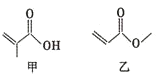
| A. | 甲、乙互为同分异构体 | |
| B. | 一定条件下,甲、乙均能发生取代反应 | |
| C. | 甲、乙都能与金属钠反应生成氢气 | |
| D. | 甲、乙都能使酸性KMnO4溶液褪色 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
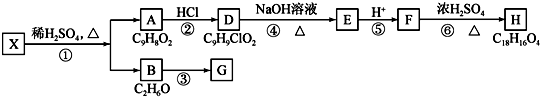
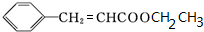 +H2O$→_{△}^{稀硫酸}$
+H2O$→_{△}^{稀硫酸}$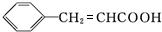 +CH3CH2OH.检验A中非含氧官能团所用的试剂为溴水或溴的四氯化碳溶液.
+CH3CH2OH.检验A中非含氧官能团所用的试剂为溴水或溴的四氯化碳溶液.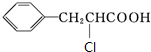 .
.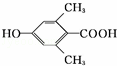 、
、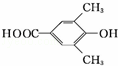 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com