
| 编号 | HA | BOH | 溶液的体积关系 |
| ① | 强酸 | 强碱 | V(HA)<V(BOH) |
| ② | 强酸 | 强碱 | V(HA)=V(BOH) |
| ③ | 强酸 | 弱碱 | V(HA)>V(BOH) |
| ④ | 弱酸 | 强碱 | V(HA)>V(BOH) |
| A. | ①③ | B. | ②③ | C. | ②④ | D. | ①④ |
分析 常温下,某酸HA溶液和某碱BOH溶液的pH之和为14,说明酸溶液中氢离子浓度与碱溶液中的氢离子浓度相等,两溶液中混合后溶液的pH=7,则反应后溶液为中性,
若为一元强酸与一元强碱溶液混合时,二者浓度相同,反应后溶液为中性,则两溶液体积相同;若酸为强酸,碱溶液为弱碱时,混合液为中性时酸溶液体积稍大;若酸为弱酸、碱为强碱时,碱溶液应该稍过量,据此进行解答.
解答 解:常温下,某酸HA溶液和某碱BOH溶液的pH之和为14,说明酸溶液中氢离子浓度与碱溶液中的氢离子浓度相等,两溶液中混合后溶液的pH=7,则反应后溶液为中性,
若都是强电解质,则两溶液浓度相同,反应后溶液为中性时溶液体积一定相等,即:V(HA)=V(BOH),故①错误、②正确;
若HA为强酸,BOH为弱碱,要满足反应后溶液为中性,则酸溶液体积应该稍大些,即:V(HA)>V(BOH),故③正确;
若HA为弱酸、BOH为弱碱时,碱的浓度大于酸,而反应后溶液为中性,则碱溶液体积稍大,即:V(HA)<V(BOH),故④错误;
故选B.
点评 本题考查了酸碱混合的定性判断及溶液pH的计算,题目难度中等,根据题干信息明确酸溶液中氢离子浓度与碱溶液中的氢离子浓度相等为解答关键,试题培养了学生的分析能力及灵活应用能力.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | CH3COOH溶液中CH3COOH的电离:CH3COOH=H ++CH3COO- | |
| B. | 用CuCl2溶液做导电实验,灯泡发光:CuCl2$\frac{\underline{\;电解\;}}{\;}$Cu2++2Cl- | |
| C. | NaHCO3溶液中HCO3-的水解:HCO3-+H2 O?H3 O ++CO32- | |
| D. | 将FeCl3溶液滴入Na2CO3溶液中:2Fe3++3 CO32?+3 H2 O═2Fe(OH)3↓+3 CO2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | △H=+488.3 kJ•mol-1 | B. | △H=-244.15 kJ•mol-1 | ||
| C. | △H=-977.6 kJ•mol-1 | D. | △H=-488.3 kJ•mol-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 碳酸氢钠溶液中滴加稀盐酸 | B. | 硫酸铁溶液中滴加硫氰化钾溶液 | ||
| C. | 碘水中滴加淀粉碘化钾溶液 | D. | 氯化铁溶液中加入还原性铁粉 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
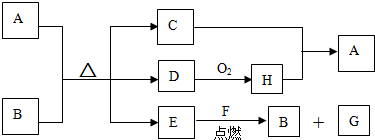
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②④⑤ | B. | ①②⑥⑦ | C. | ③⑤⑦ | D. | ②③⑤⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 该反应中X物质为O2 | |
| B. | 反应物Na2O2只做氧化剂 | |
| C. | 该反应中发生氧化反应的过程只有FeSO4→Na2FeO4 | |
| D. | 每生成lmol Na2FeO4,反应过程中转移4 mol e- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 硼、铝、镓 | B. | 氮、磷、砷 | C. | 铜、银、金 | D. | 锌、镉、汞 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH3CH2Br+NaOH$→_{△}^{H_{2}O}$CH2=CH2↑+NaBr+H2O | |
| B. | 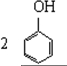 +3Br2→ +3Br2→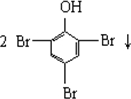 | |
| C. | nCH2=CH-CH3$\stackrel{一定条件}{→}$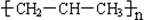 | |
| D. | CH3CHO+NaOH+2Cu(OH)2$\stackrel{加热}{→}$ CH3COONa+Cu2O↓+3H2O. |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com