
| A. | 3d3表示3d能级上有3个轨道 | |
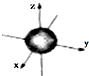
| B. | ns能级的原子轨道图都可以用右图表示 | |
| C. | 1s电子云呈球形,表示电子绕原子核做圆周运动 | |
| D. | 电子云图的黑点密度越大,说明核外空间电子数越多 |
分析 A.d3中的3表示d能级上的电子个数;
B.电子云的轮廓图称为原子轨道;
C.电子云表示表示电子在核外空间某处出现的机会;
D.小黑点的疏密表示电子出现机会的多少.
解答 解:A.3d3表示3d能级有3个电子,故A错误;
B.ns能级的电子云呈球形,所以可以用该图表示该能级的原子轨道,故B正确;
C.电子云表示表示电子在核外空间某处出现的机会,不代表电子的运动轨迹,故C错误;
D.小黑点的疏密表示电子出现机会的多少,密则机会大,疏则机会小,故D错误;
故选B.
点评 本题考查了电子云、原子轨道等知识点,易错选项是C,注意电子云中小黑点的疏密表示电子出现机会的多少,而不表示电子的数目,为易错点.


 天天练口算系列答案
天天练口算系列答案科目:高中化学 来源: 题型:解答题
| 元素编号 | 元素性质或原子结构 |
| T | 最外层电子数比内层电子总数少4 |
| X | 最外层电子数是次外层电子数的2倍 |
| Y | 与氢形成的气态化合物在标准状况下的密度为0.76g•L-1 |
| Z | 元素最高正价与负价的绝对值之差是6 |
 .
. .
. ,
, .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
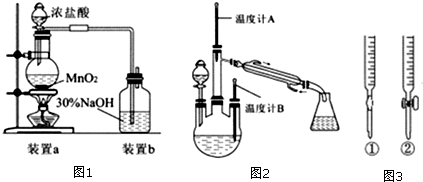
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 供电时的总反应是:2H2+O2=2H2O | |
| B. | 产物为无污染的水,属于环境友好电池 | |
| C. | 燃料电池的能量转化率无法达到100% | |
| D. | H2在负极发生还原反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | HClO的结构式:H-O-Cl | B. | 纯碱的化学式为:Na2CO3 | ||
| C. | 原子核内有8个中子的碳原子148C | D. | Na2O2电子式为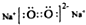 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
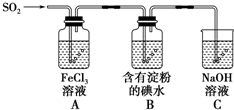 某兴趣小组探究SO2气体还原Fe3+、I2,它们使用的药品和装置如图所示
某兴趣小组探究SO2气体还原Fe3+、I2,它们使用的药品和装置如图所示查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com