
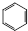
 +HNO3$\stackrel{����}{��}$
+HNO3$\stackrel{����}{��}$ +H2O����Ӧ����ȡ����Ӧ
+H2O����Ӧ����ȡ����Ӧ���� ��1����ϩ�ڴ��������·����ӳɷ�Ӧ�����Ҵ���
��2������������Ӧ�DZ���Ũ���ᡢŨ������ȷ�����ȡ����Ӧ������������
��3���Ҵ���������Ũ������ȷ�Ӧ��������������ˮ��
��4�����������ڼ��������µ�ˮ�����������ƺ��Ҵ���
��5������ȼ�����ɶ�����̼��ˮ��
��� �⣺��1����ϩ��H2O��Ӧ�ڴ��������·����ӳɷ�Ӧ�����Ҵ�����Ӧ�Ļ�ѧ����ʽΪ��CH2=CH2+H2O$��_{��}^{����}$CH3CH2OH����Ӧ����Ϊ�ӳɷ�Ӧ��
�ʴ�Ϊ��CH2=CH2+H2O$��_{��}^{����}$CH3CH2OH���ӳɷ�Ӧ��
��2������Ũ���ᡢŨ������ȷ�����ȡ����Ӧ��������������Ӧ�Ļ�ѧ����ʽΪ�� +HNO3$\stackrel{����}{��}$
+HNO3$\stackrel{����}{��}$ +H2O����Ӧ����Ϊȡ����Ӧ��
+H2O����Ӧ����Ϊȡ����Ӧ��
�ʴ�Ϊ�� +HNO3$\stackrel{����}{��}$
+HNO3$\stackrel{����}{��}$ +H2O��ȡ����Ӧ��
+H2O��ȡ����Ӧ��
��3���Ҵ���������Ũ������ȷ�Ӧ��������������ˮ����Ӧ�Ļ�ѧ����ʽΪ��CH3COOH+C2H5OH$?_{��}^{Ũ����}$CH3COOC2H5+H2O����Ӧ����Ϊ������Ӧ��ȡ����Ӧ��
�ʴ�Ϊ��CH3COOH+C2H5OH$?_{��}^{Ũ����}$CH3COOC2H5+H2O��������Ӧ��ȡ����Ӧ��
��4�����������ڼ��������µ�ˮ�����������ƺ��Ҵ�����Ӧ����Ϊˮ�ⷴӦ��ȡ����Ӧ��
�ʴ�Ϊ��CH3COOCH2CH3+NaOH$\stackrel{��}{��}$CH3COONa+CH3CH2OH��ˮ�ⷴӦ��ȡ����Ӧ��
��5������ȼ�շ���������Ӧ��������Ӧ���ɶ�����̼��ˮ����Ӧ�Ļ�ѧ����ʽΪ��CH4+2O2$\stackrel{��ȼ}{��}$CO2+2H2O����Ӧ����Ϊ������Ӧ��
�ʴ�Ϊ��CH4+2O2$\stackrel{��ȼ}{��}$CO2+2H2O��������Ӧ��
���� ���⿼�����������ʡ���Ӧ��������Ӧ�����Ӧ���͵ķ����жϣ�ע�⻯ѧ����ʽ��д������ע�����⣬���������ǽ���ؼ�����Ŀ�ϼ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

 ��
�� ��
��
 ��
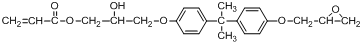
��
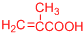 ����
����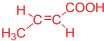 ��
��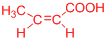 ����
�����鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | C2H4 | B�� | CH��CH | C�� | CH3C��CH | D�� | CH4 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �������;ƾ� | B�� | �屽���� | C�� | �ױ���ˮ | D�� | �������ͼ��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��ԭ��Na��Mg��Al | B�� | ������Cl2��S��P | ||
| C�� | ����H2SO4��H3PO4��HClO4 | D�� | �ȶ���HCl��H2S��PH3 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ������BN�����������ǽ������ϣ������������ͻ���Ϻͳ�Ӳ���ϵȣ�ij��ȤС������װ����NH3��B2O3�����ڸ������Ʊ�����������
������BN�����������ǽ������ϣ������������ͻ���Ϻͳ�Ӳ���ϵȣ�ij��ȤС������װ����NH3��B2O3�����ڸ������Ʊ������������鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
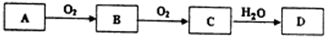
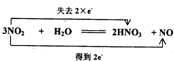
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com