
下列说法正确的是( )
A.常温下,将pH=3的醋酸溶液稀释到原体积的10倍后,溶液的pH=4
B.为确定某酸H2A是强酸还是弱酸,可测NaHA溶液的pH。若pH>7,则H2A是弱酸;若pH<7,则H2A是强酸
C.用0.2000 mol·L-1 NaOH标准溶液滴定HCl与CH3COOH的混合液(混合液中两种酸的浓度均约为0.1 mol·L-1),至中性时,溶液中的酸未被完全中和
D.相同温度下,将足量氯化银固体分别放入相同体积的①蒸馏水、②0.1 mol·L-1盐酸、③0.1 mol·L-1氯化镁溶液、④0.1 mol·L-1硝酸银溶液中,Ag+浓度:①>④=②>③
C
【解析】 醋酸溶液中存在CH3COOH CH3COO-+H+,加水稀释时,电离平衡向右移动,故将pH=3的醋酸溶液稀释10倍,其pH小于4,但大于3,A项不正确;若H2A是弱酸,则HA-在溶液中存在两个平衡:HA-
CH3COO-+H+,加水稀释时,电离平衡向右移动,故将pH=3的醋酸溶液稀释10倍,其pH小于4,但大于3,A项不正确;若H2A是弱酸,则HA-在溶液中存在两个平衡:HA- H++A2-(电离平衡),HA-+H2O??H2A+OH-(水解平衡),电离程度和水解程度的相对大小决定了溶液的酸碱性,如NaHCO3溶液显碱性,NaHSO3溶液显酸性,故B项不正确;完全中和时,生成正盐NaCl和CH3COONa,由于CH3COO-的水解而使溶液显碱性,故溶液呈中性时酸未被完全中和,C项正确;氯化银的溶度积常数表达式为Ksp=c(Ag+)·c(Cl-),c(Cl-)越大,c(Ag+)越小,故Ag+浓度大小顺序应为:④>①>②>③,D项不正确。
H++A2-(电离平衡),HA-+H2O??H2A+OH-(水解平衡),电离程度和水解程度的相对大小决定了溶液的酸碱性,如NaHCO3溶液显碱性,NaHSO3溶液显酸性,故B项不正确;完全中和时,生成正盐NaCl和CH3COONa,由于CH3COO-的水解而使溶液显碱性,故溶液呈中性时酸未被完全中和,C项正确;氯化银的溶度积常数表达式为Ksp=c(Ag+)·c(Cl-),c(Cl-)越大,c(Ag+)越小,故Ag+浓度大小顺序应为:④>①>②>③,D项不正确。


 黄冈天天练口算题卡系列答案
黄冈天天练口算题卡系列答案科目:高中化学 来源:2015届吉林省高二3月月考化学试卷(解析版) 题型:选择题
下列实验能达到预期目的的是
A.向煮沸的1 mol·L-1 NaOH溶液中滴加FeCl3饱和溶液制备Fe(OH)3胶体
B.用氢氧化铜粉末检测尿糖
C.称取19.0 g SnCl2,用100 mL蒸馏水,配制1.0 mol·L-1 SnCl2溶液
D.向乙酸乙酯中加入饱和Na2CO3溶液,振荡,分液分离除去乙酸乙酯中的少量乙酸
查看答案和解析>>
科目:高中化学 来源:2015届北京市怀柔区高二上学期期末质量检测化学试卷(解析版) 题型:选择题
居室空气污染的主要来源之一是人们使用的装饰材料、胶合板、内墙涂料释放出的一种刺激性气味的气体,该气体是
A.CH4 B.NH3 C.HCHO D.SO2
查看答案和解析>>
科目:高中化学 来源:2014高考化学苏教版总复习 专题9有机化合物的获取与应用练习卷(解析版) 题型:选择题
下列每组中各有三对物质,它们都能用分液漏斗分离的是( )
A.乙酸乙酯和水、乙醇和水、葡萄糖和水
B.甘油和水、乙醛和水、乙酸和乙醇
C.乙酸乙酯和水、溴苯和水、硝基苯和水
D.乙酸和水、甲苯和水、己烷和水
查看答案和解析>>
科目:高中化学 来源:2014高考化学苏教版总复习 专题8溶液中的离子反应练习卷(解析版) 题型:填空题
(1)将0.15 mol·L-1稀硫酸V1 mL与0.1 mol·L-1 NaOH溶液V2 mL混合,所得溶液的pH为1,则V1:V2=________。(溶液体积变化忽略不计)
(2)常温下,某水溶液中存在的离子有:Na+、A-、H+、OH-,据题意,回答下列问题:
①若该水溶液由0.1 mol·L-1 HA溶液与0.1 mol·L-1NaOH溶液等体积混合而得,则溶液的pH________7。
②若溶液pH>7,则c(Na+)________c(A-),理由是________。
③若该溶液由pH=3的HA溶液V1 mL与pH=11的NaOH溶液V2 mL混合而得,则下列说法正确的是________。
A.若反应后溶液呈中性,则c(H+)+c(OH-)=2×10-7mol·L-1
B.若V1=V2,反应后溶液pH一定等于7
C.若反应后溶液呈酸性,则V1一定大于V2
D.若反应后溶液呈碱性,则V1一定小于V2
查看答案和解析>>
科目:高中化学 来源:2014高考化学苏教版总复习 专题8溶液中的离子反应练习卷(解析版) 题型:选择题
室温下,取0.2 mol·L-1CH3COOH溶液与0.2 mol·L-1 NaOH溶液等体积混合(忽略混合后溶液体积的变化),测得混合溶液的pH=8,则下列说法(或关系式)正确的是( )
A.混合溶液中由水电离出的c(H+)=10-8 mol·L-1
B.溶液中离子浓度由大到小的顺序为c(CH3COO-)>c(Na+)>c(OH-)>c(H+)
C.混合溶液中c(Na+)=c(CH3COOH)+c(CH3COO-)=0.2 mol·L-1
D.混合溶液中c(OH-)-c(CH3COOH)=c(H+)=1×10-8 mol·L-1
查看答案和解析>>
科目:高中化学 来源:2014高考化学苏教版总复习 专题8溶液中的离子反应练习卷(解析版) 题型:选择题
某同学取等体积的稀盐酸与稀醋酸各一份进行稀释,下面是稀释前后的有关数据及结论,其中肯定错误的是( )
ABCD
稀释前酸浓度相同酸浓度相同pH均为3pH均为3
稀释量均为10倍稀释至两酸pH相同稀释至pH均为5均为100倍
结论pH:盐酸的小稀释倍数:盐酸的大稀释倍数:盐酸的大pH:盐酸的大
查看答案和解析>>
科目:高中化学 来源:2014高考化学苏教版总复习 专题7化学反应速率与化学平衡练习卷(解析版) 题型:选择题
在密闭的容器中进行如下反应:H2(g)+I2(g)  2HI(g),在温度T1和T2时,产物的量和时间的关系如图所示,根据图像判断正确的是( )
2HI(g),在温度T1和T2时,产物的量和时间的关系如图所示,根据图像判断正确的是( )
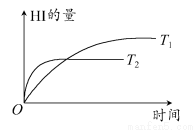
A.T1<T2,ΔH<0 B.T1>T2,ΔH<0 C.T1<T2,ΔH>0 D.T1>T2,ΔH>0
查看答案和解析>>
科目:高中化学 来源:2014高考化学苏教版总复习 专题5微观结构与物质的多样性练习卷(解析版) 题型:选择题
短周期元素甲、乙、丙、丁、戊五种元素在元素周期表中的位置如右图所示,其中戊是同周期中原子半径最小的元素。下列有关判断正确的是( )
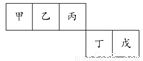
A.最外层电子数:甲>乙>丙>丁>戊
B.简单离子的离子半径:戊>丁
C.含有丁元素的酸有多种
D.乙的氢化物多种多样,丙、丁、戊的氢化物各有一种
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com