
 .
. 分析 A、B、C、D、E、F、G 七种前四周期元素,G 的原子序数最大;C 的气态单质在标准状况下每升的质量为3.17g,其摩尔质量=3.17g/L×22.4L=71g/mol,为Cl元素;
A、B、C 三种元素的原子次外层电子排布都是(n-1)s2(n-1)p6,则n=3,A、B、C都属于第三周期元素;A 与C 能形成离子化合物AC,A 离子比C 离子少一个能层,则A是Na元素;
E 原子的最外电子层中p 能级的电子数等于前一能层的电子总数,则E是C元素;
D、E、F 三种元素的原子序数分别等于A、B、C 的最外层电子数,则B原子最外层电子数为6,为S元素,D是H元素,F是N元素;
G 元素原子的最外层电子数和A 相同,内层电子排布均符合2n2,为Cu元素,
所以A、B、C、D、E、F、G 七种元素分别是Na、S、Cl、H、C、N、Cu元素,再结合题目分析解答.
解答 解:A、B、C、D、E、F、G 七种前四周期元素,G 的原子序数最大;C 的气态单质在标准状况下每升的质量为3.17g,其摩尔质量=3.17g/L×22.4L=71g/mol,为Cl元素;
A、B、C 三种元素的原子次外层电子排布都是(n-1)s2(n-1)p6,则n=3,A、B、C都属于第三周期元素;A 与C 能形成离子化合物AC,A 离子比C 离子少一个能层,则A是Na元素;
E 原子的最外电子层中p 能级的电子数等于前一能层的电子总数,则E是C元素;
D、E、F 三种元素的原子序数分别等于A、B、C 的最外层电子数,则B原子最外层电子数为6,为S元素,D是H元素,F是N元素;
G 元素原子的最外层电子数和A 相同,内层电子排布均符合2n2,为Cu元素,
所以A、B、C、D、E、F、G 七种元素分别是Na、S、Cl、H、C、N、Cu元素,
(1)上述元素的基态原子中,含有2 个未成对电子的元素是C(填元素符号);它们位于元素周期表的sp区,故答案为:C;sp;
(2)A 与D 能形成离子化合物AD为NaH,为离子晶体,AD 的电子式是Na+[:H]-,
故答案为:Na+[:H]-;
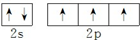
(3)C是Cl元素,C 元素基态原子的价电子为3s、3p电子,其价电子排布式为3s23p5,F 元素是N元素,N原子基态原子最外层电子的轨道表示式为 ,
,
故答案为:3s23p5; .
.
点评 本题考查位置结构相互关系及运用,为高频考点,涉及元素推断、原子核外电子排布、电子式的书写等知识点,侧重考查学生推断及基本知识应用,正确推断元素是解本题关键,熟练掌握原子核外电子排布及元素周期表结构,题目难度不大.


科目:高中化学 来源: 题型:推断题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 烧碱、液态氧、碘酒 | B. | 生石灰、白磷、熟石灰 | ||
| C. | 干冰、铁、氯化氢 | D. | 纯碱、氮气、氧气 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 除去水中的HClO | B. | 紫外线杀菌消毒 | C. | 增加水中含氧量 | D. | 提高水温 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 摩尔是物质的量的单位 | |
| B. | 物质的量的符号是M | |
| C. | H2的摩尔质量是2g | |
| D. | NA表示阿伏加德罗常数,lmolCl2含有2NA个氯原子 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 胶体是很稳定的分散系,比溶液还稳定 | |
| B. | 胶体能发生丁达尔现象 | |
| C. | 胶体的分散质不能透过滤纸 | |
| D. | 胶体不稳定,静止后容易产生沉淀 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NaHCO3(溶液):NaHCO3═Na++H++CO32- | |
| B. | NaHSO4(溶液):NaHSO4═Na++H++SO42- | |
| C. | (NH4)2SO4(溶液):(NH4)2SO4═(NH4)2++SO42- | |
| D. | CuCl2(溶液):CuCl2═Cu2++Cl2- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
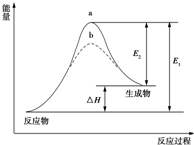
| A. | 该反应的反应热△H=E2-E1 | B. | 该反应为放热反应 | ||
| C. | 催化剂能改变反应的活化能 | D. | 催化剂能改变反应的焓变 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 把NaHCO3和Na2CO3混和物6.85g溶于水制成100mL溶液,其中c(Na+)=1mol•L-1.该溶液中加入一定量盐酸恰好完全反应,将溶液蒸干后,所得固体质量无法计算 | |
| B. | 将54.4g铁粉和氧化铁的混合物中加入4.0mol/L 200mL的稀硫酸,恰好完全反应,放出氢气4.48L(标准状况).反应后的溶液中滴加KSCN不显红色,且无固体剩余物,反应后得到FeSO4的物质的量是0.8mol | |
| C. | 现向一密闭容器中充入1molN2和3molH2,在一定条件下使该反应发生,达到化学平衡时,N2、H2和NH3的物质的量浓度一定相等 | |
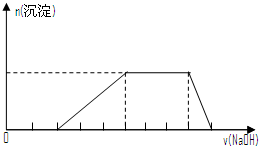
| D. | 某溶液中可能含有H+、Na+、NH${\;}_{4}^{+}$、Mg2+、Fe3+、Al3+、SO${\;}_{4}^{2-}$等离子,当向该溶液中加入某浓度的NaOH溶液时,发现生成沉淀的物质的量随NaOH溶液的体积变化如图所示,由此可知,该溶液中肯定含有的阳离子是H+、NH${\;}_{4}^{+}$、Mg2+、Al3+ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com