
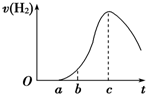
 把在空气中久置的铝片5.0g投入盛有500mL 0.5mol?L-1硫酸溶液的烧杯中,该铝片与硫酸反应产生氢气的速率与反应时间的关系可用如图曲线来表示,回答下列问题:
把在空气中久置的铝片5.0g投入盛有500mL 0.5mol?L-1硫酸溶液的烧杯中,该铝片与硫酸反应产生氢气的速率与反应时间的关系可用如图曲线来表示,回答下列问题:

 教学练新同步练习系列答案
教学练新同步练习系列答案 课前课后同步练习系列答案
课前课后同步练习系列答案 课堂小作业系列答案
课堂小作业系列答案 黄冈小状元口算速算练习册系列答案
黄冈小状元口算速算练习册系列答案 成功训练计划系列答案
成功训练计划系列答案 倍速训练法直通中考考点系列答案
倍速训练法直通中考考点系列答案科目:高中化学 来源: 题型:
| A、硅的非金属性比碳强,只有在高温下才能跟氢气起化合反应 |
| B、硅是构成矿物和岩石的主要元素,硅在地壳中的含量在所有的元素中居第一位 |
| C、硅的化学性质不活泼,在自然界中可以以游离态存在 |
| D、硅在电子工业中是重要的半导体材料 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、H2SO4、HNO3 |
| B、HCl、HNO3 |
| C、HCl、H2SiO3、 |
| D、HCl、H2SO4 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、上述反应中水是氧化剂 |
| B、若反应过程中转移5 mol e-则生成标准状况下N2的体积为11.2L |
| C、该反应的氧化产物是N2 |
| D、当消耗1 mol Al时,生成标况下N2的体积为22.4L |
查看答案和解析>>
科目:高中化学 来源: 题型:
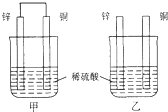 原电池原理的发现是储能和供能技术的巨大进步,是化学对人类的一项重大贡献.
原电池原理的发现是储能和供能技术的巨大进步,是化学对人类的一项重大贡献.查看答案和解析>>
科目:高中化学 来源: 题型:
| A、COS属于离子化合物 |
| B、COS分子中,所有原子都满足8电子的稳定结构 |
| C、COS的结构式为O=C-S |
| D、COS含有共价键 |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、
| ||
B、1.993×
| ||
C、
| ||
D、9.288×
|
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com