
| A、在任何条件下,化学平衡常数K都是一个定值 |
| B、当改变反应物的浓度时,化学平衡常数会发生改变 |
| C、化学平衡常数K只与温度有关,与反应物浓度、体系的压强无关 |
| D、化学平衡常数K与反应物的转化率是一一对应的 |


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
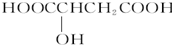 具有健脾作用.下列有关说法正确的是( )
具有健脾作用.下列有关说法正确的是( )| A、该羟基酸含有3种官能团 |
| B、通常条件下,该羟基酸可以发生取代、氧化和加成反应 |
| C、该羟基酸可以在Cu的催化下被O2氧化成醛 |
| D、含1mol该羟基酸的溶液可与含2mol氢氧化钠的溶液恰好完全反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
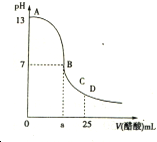 25℃时,在25mL 0.1mol?L-1的NaOH 溶液中,逐滴加入0.2mol?L-1的CH3COOH 溶液,溶液的pH 与醋酸溶液体积关系如图.下列分析正确的是( )
25℃时,在25mL 0.1mol?L-1的NaOH 溶液中,逐滴加入0.2mol?L-1的CH3COOH 溶液,溶液的pH 与醋酸溶液体积关系如图.下列分析正确的是( )| A、B 点的横坐标a=12.5 |
| B、C 点时溶液中有:c(Na+)>c(CH3COO-)>c(H+)>c(OH-) |
| C、D 点时溶液中有:2c(Na+)=c(CH3COO-)+c(CH3COOH) |
| D、曲线上A、B 间的任意一点,溶液中都有:c(CH3COO-)>c(Na+)>c(OH-)>c(H+) |
查看答案和解析>>
科目:高中化学 来源: 题型:
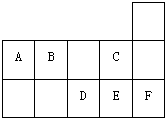
| A、A、B、D、E四种元素所形成的最高价含氧酸中D酸性最强 |
| B、形成的简单阴离子半径:C>B>D>E |
| C、D、E、F形成的单质都是双原子分子 |
| D、A与E形成的分子是一种常见有机溶剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、200 mL 0.1 mol/L NH4Cl 溶液 |
| B、50 mL 0.2 mol/L NH4NO3溶液 |
| C、100 mL 0.2 mol/L NH4HSO4 |
| D、50 mL 0.2 mol/L氨水 |
查看答案和解析>>
科目:高中化学 来源: 题型:
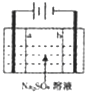 近来人们开发了通过电解同时生产NaOH和H2SO4的化学工艺,现在用离子交换膜(a、b)和石墨作电极的电解池进行生产模根,下列主产法中不正确的是( )
近来人们开发了通过电解同时生产NaOH和H2SO4的化学工艺,现在用离子交换膜(a、b)和石墨作电极的电解池进行生产模根,下列主产法中不正确的是( )| A、阴极反应式4OH--4e-=2H2O+O2↑ |
| B、阴极得到NaOH,阳极得到H2SO4 |
| C、每生产1molH2SO4,同时得到2mol NaOH |
| D、此反应实质就是电解水 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、ⅰ中碘为气态,ⅱ中碘为固态 |
| B、反应(ⅰ)的产物比反应(ⅱ)的产物稳定 |
| C、1 mol I2(g)中通入1 mol H2(g),反应放热9.48 kJ |
| D、1 mol固态碘与1 mol气态碘所含的能量相差17.00 kJ |
查看答案和解析>>
科目:高中化学 来源: 题型:

| 红磷 |
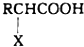 +HX
+HX查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com