
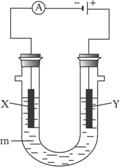
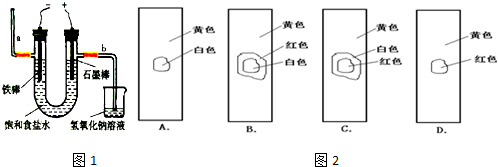
A.X电极为阳极,Y电极为阴极
B.X电极溶液变红色,且有刺激性气味气体产生
C.若将X、Y两极产生的气体收集起来,其体积比略大于1∶1
D.电解后,将溶液混匀,电解前后溶液的pH未发生变化
科目:高中化学 来源: 题型:阅读理解
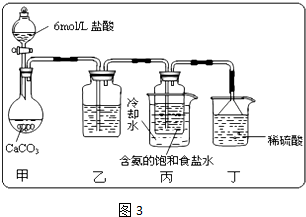
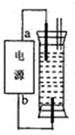 (2009?江门一模)某研究性学习小组设计了一个环保型消毒液发生器,如图所示装置,用一石墨作电极电解饱和NaCl溶液,请你完成以下实验探究过程:
(2009?江门一模)某研究性学习小组设计了一个环保型消毒液发生器,如图所示装置,用一石墨作电极电解饱和NaCl溶液,请你完成以下实验探究过程:
| ||
| ||
| 假设 | 实验操作 | 预期现象 | 结论 |
| ①有明显现象 | 用烧杯取少量消毒液,将一颗光亮的铁钉放入烧杯,浸泡一段时间 用烧杯取少量消毒液,将一颗光亮的铁钉放入烧杯,浸泡一段时间 |
铁定表面出现铁锈 铁定表面出现铁锈 |
铁定被锈蚀 铁定被锈蚀 |
| ②无明显现象,要进一步探究 | 用试管取少量(实验①)浸泡后的溶液,滴加足量的1mol/L的硫酸酸化,再用滴管滴加几滴20%的KSCN溶液 用试管取少量(实验①)浸泡后的溶液,滴加足量的1mol/L的硫酸酸化,再用滴管滴加几滴20%的KSCN溶液 |
溶液不变色或溶液显血红色 溶液不变色或溶液显血红色 |
铁钉可能未被腐蚀也可能被腐蚀 铁钉可能未被腐蚀也可能被腐蚀 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
| ||
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com