
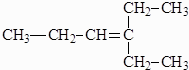 一种有机化合物的结构简式为:
一种有机化合物的结构简式为:分析 (1)甲基、亚甲基、次甲基中的C原子为sp3杂化,C=C中的C原子为sp2杂化;
(2)甲基、亚甲基、次甲基中的C原子为sp3杂化,形成sp3杂化轨道,C=C中的C原子为sp2杂化,形成sp2杂化轨道,根据分子中成键的方式判断.
解答 解:(1)甲基、亚甲基、次甲基中的C原子为sp3杂化,C=C中的C原子为sp2杂化,所以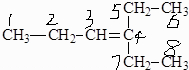 中1、2、5、6、7、8号共6个碳原子sp3杂化;3、4号共2个碳原子sp2杂化;
中1、2、5、6、7、8号共6个碳原子sp3杂化;3、4号共2个碳原子sp2杂化;
故答案为:2;6;
(2)甲基、亚甲基、次甲基中的C原子为sp3杂化,形成sp3杂化轨道,C=C中的C原子为sp2杂化,形成sp2杂化轨道,所以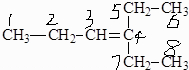 中1和2、5和6、7和8号碳原子间
中1和2、5和6、7和8号碳原子间
为sp3-sp3的σ键;2和3、4和5、4和7号碳原子间为sp2-sp3的σ键;
故答案为:3;3.
点评 本题考查有机物的化学键,明确化学键的判断规律及分子的结构等即可解答,杂化类型为解答的易错点,题目难度不大.


 寒假大串联黄山书社系列答案
寒假大串联黄山书社系列答案科目:高中化学 来源: 题型:选择题
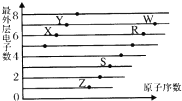 如图是部分短周期元素原子(用字母表示)最外层电子数与原子序数的关系图.下列说法正确的是( )
如图是部分短周期元素原子(用字母表示)最外层电子数与原子序数的关系图.下列说法正确的是( )| A. | 该图体现出原子核外电子层呈现周期性变化 | |
| B. | 简单离子半径:W->R2->Z+>S3+ | |
| C. | R、Z形成的化合物中可能含有共价键 | |
| D. | 由酸性:HWO4>H2RO3可证明非金属性:W>R |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
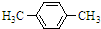 +Br2$\stackrel{FeBr_{3}}{→}$
+Br2$\stackrel{FeBr_{3}}{→}$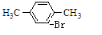 +HBr.
+HBr.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
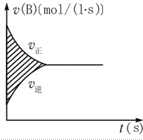
| A. | A浓度的减小量 | B. | B浓度的减小量 | ||
| C. | C物质的量的增加量 | D. | B物质的量的减少量 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 因为H-F的键能大于H-CI,所以HF的沸点高于HCI | |
| B. | 因为HCIO4比HCIO中的氯元素的化合价高,所以HCIO4的氧化性强于HCIO | |
| C. | 因为N元素的非金属性比P元素强,所以NH3的稳定性强于PH3 | |
| D. | 因为Fe的还原性强于Cu,所以Cu2+的氧化性强于Fe3+ |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
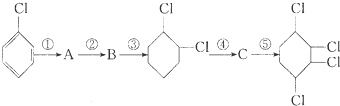
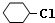 ,B:
,B: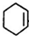 ,C:
,C: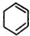 .
.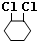 +2NaOH$→_{△}^{醇}$
+2NaOH$→_{△}^{醇}$ +2NaCl+2H2O、
+2NaCl+2H2O、 +2Cl2→
+2Cl2→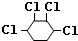 .
.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.11mol | B. | 0.22mol | C. | 0.16mol | D. | 0.1mol |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com