
(2004·潍坊)根据下列叙述回答①、②题.
能源可划分为一级能源和二级能源,自然界中以现成形式提供的能源称为一级能源;需要依靠其他能源的能量间接制取的能源称为二级能源.氢气是一种高效而没有污染的二级能源,它可以由自然界中大量存在的水来制取:
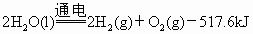
(1)下列叙述正确的是
[ ]
A.电能是二级能源
B.水力是二级能源
C.天然气是一级能源
D.焦炉气是一级能源
(2)关于用水制取二级能源氢气,以下研究方向正确的是
[ ]
A.构成水的氢和氧都是可以燃烧的物质,因此可研究在水不分解的情况下使氢成为二级能源
B.设法将太阳光聚集产生高温,使水分解产生氢气
C.寻找高效催化剂,使水分解产生氢气,同时释放能量
D.寻找特殊化学物质,用于开发廉价能源,以分解水制取氢气
|
解析: (1)此题是一道信息给予题,考查二级能源的概念.根据能源的划分原则,电能和焦炉气很明显是由其他能源如火力、水力、原子能或炼焦等能源转变而来的,因而它们属于二级能源.水力是一级能源,天然气是一级能源.(2) 此题主要考查学生分析问题的能力及审题能力.由题给信息可知,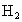 是可以燃烧的,但水中的氢元素不可燃烧,因此必须使水分解产生 是可以燃烧的,但水中的氢元素不可燃烧,因此必须使水分解产生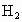 ,又因 ,又因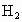 和 和 化合生成水是放热反应,故由 化合生成水是放热反应,故由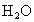 来制取 来制取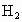 必须外界提供能量,无论选用何种高效催化剂也不会使水分解产生 必须外界提供能量,无论选用何种高效催化剂也不会使水分解产生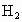 的同时释放能量,故C是不正确的. 的同时释放能量,故C是不正确的.
仔细分析 A选项,构成水的氢和氧都是可燃烧的物质,显然这句话有问题,因为氧元素无论是游离态或是化合态都不是可燃物质,氧气只可以助燃.根据能量守恒原理,水要变为氢气,必须吸收外界能量,才能使水分解产生氢气,在水不分解的情况下,绝对不可能产生氢气,故A选项也是错误的.无论使用太阳能,还是利用其他特殊物质提供的能量,使水分解产生氢气都是可能的,所以B、D正确. |


 金牌教辅培优优选卷期末冲刺100分系列答案
金牌教辅培优优选卷期末冲刺100分系列答案科目:高中化学 来源: 题型:
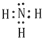
查看答案和解析>>
科目:高中化学 来源: 题型:
| 滴定次数 | 待测溶液体积(mL) | 标准酸体积 | |
| 滴定前的刻度(mL) | 滴定后的刻度(mL) | ||
| 第一次 | 10.00 | 0.40 | 20.50 |
| 第二次 | 10.00 | 4.10 | 24.00 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| NaCl | MgCl2 | AlCl3 | SiCl4 | 单质B | |
| 熔点(℃) | 801 | 714 | 190 | -70 | 2300 |
| 沸点(℃) | 1413 | 1412 | 180 | 57 | 2500 |
| A、NaCl比MgCl2更容易熔化 |
| B、单质B可能是原子晶体 |
| C、AlCl3在加热时能升华 |
| D、SiCl4是分子晶体 |
查看答案和解析>>
科目:高中化学 来源: 题型:013
(2004·潍坊)在一真空、密闭容器中盛有n mol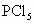 ,在200℃时发生如下反应:
,在200℃时发生如下反应:
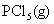
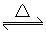
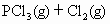 反应达平衡时,
反应达平衡时, 所占的体积分数为M%,若在同一温度下,同一容器中,最初投入的是2n mol
所占的体积分数为M%,若在同一温度下,同一容器中,最初投入的是2n mol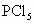 ,反应达平衡时,
,反应达平衡时, 的体积分数为N%,则M和N的关系是
的体积分数为N%,则M和N的关系是
[ ]
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com