
| A、分散系中分散质粒子的直径:Fe(OH)3悬浊液>Fe(OH)3胶体>FeCl3溶液 |
| B、能自发进行的化学反应,一定是△H<0、△S>0 |
| C、焰色反应是物质燃烧时火焰呈现的颜色变化,属于化学变化 |
| D、钢铁发生电化学腐蚀时,负极的电极反应式为 Fe-3e-=Fe3+ |


科目:高中化学 来源: 题型:
| A、达到平衡时,反应物和生成物的浓度一定相等 |
| B、达到平衡时,反应物和生成物的浓度保持一定 |
| C、加入催化剂V2O5,可以使SO2更多的转化为SO3 |
| D、反应达到平衡后,该平衡不随外界条件变化而变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、碘晶体受热转变成碘蒸气,吸收的热量用于克服碘原子间的作用力 |
| B、分子晶体中都存在共价键 |
| C、氯化氢和氯化钾的溶解克服相同类型作用力 |
| D、在晶体中只要有阴离子就一定有阳离子 |
查看答案和解析>>
科目:高中化学 来源: 题型:
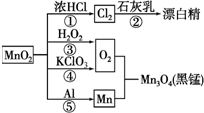
| A、反应①②③④⑤均属于氧化还原反应 |
| B、反应⑤说明该条件下铝可用于制熔点较高的金属 |
| C、相同条件下生成等量的O2,反应③和④转移的电子数之比为1:1 |
| D、反应①中氧化剂与还原剂的物质的量之比为1:4 |
查看答案和解析>>
科目:高中化学 来源: 题型:
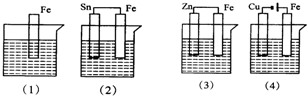 如图各容器中盛有海水,铁在其中腐蚀时由快到慢的顺序是( )
如图各容器中盛有海水,铁在其中腐蚀时由快到慢的顺序是( )| A、(4)>(2)>(1)>(3) |
| B、(2)>(1)>(3)>(4) |
| C、(4)>(2)>(3)>(1) |
| D、(3)>(2)>(4)>(1) |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
 生物质能是一种洁净、可再生能源.生物质气(主要成分为CO、CO2、H2等)与H2混合,催化合成甲醇是生物质能利用的方法之一.
生物质能是一种洁净、可再生能源.生物质气(主要成分为CO、CO2、H2等)与H2混合,催化合成甲醇是生物质能利用的方法之一.| △ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com