
NH3分子空间构型是三角锥形,而CH4是正四面体形,这是因为( )
A.两种分子的中心原子杂化轨道类型不同,NH3为sp2杂化,而CH4是sp3杂化
B.NH3分子中N原子形成3个杂化轨道,CH4分子中C原子形成4个杂化轨道
C.NH3分子中有一对未成键的孤对电子,它对成键电子的排斥作用较强
D.NH3分子中有3个σ键,而CH4分子中有4个σ键
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
某离子化合物DxEC6,晶胞结构如下图所示,阳离子D+位于正方体的棱的中点和正方体内部,阴离子EC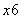 位于该正方体的顶点和面心。该化合物中x值为( )
位于该正方体的顶点和面心。该化合物中x值为( )
A.1 B.2 C.3 D.4
查看答案和解析>>
科目:高中化学 来源: 题型:
下列物质性质的变化规律,与化学键的强弱无关的是( )
A.F2、Cl2、Br2、I2的熔点、沸点逐渐升高
B.HF、HCl、HBr、HI的热稳定性依次减弱
C.金刚石的硬度、熔点、沸点都高于晶体硅
D.NaF、NaCl、NaBr、NaI的熔点依次降低
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于丙烯(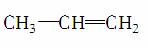 )的说法不正确的是( )
)的说法不正确的是( )
A.丙烯分子有8个σ键,1个π键
B.丙烯分子中3个碳原子都是sp3杂化
C.丙烯分子中存在非极性键
D.丙烯分子中3个碳原子不在同一直线上
查看答案和解析>>
科目:高中化学 来源: 题型:
在试管①中先加入2 mL 95%的乙醇,并在摇动下缓缓加入2 mL浓硫酸,充分摇匀,冷却后再加入2 g无水醋酸钠,用玻璃棒充分搅拌后将试管固定在铁架台上。在试管②中加入5 mL Na2CO3饱和溶液,按图示装置连接。用酒精灯对试管①加热,当观察到试管②中有明显现象时,停止实验。
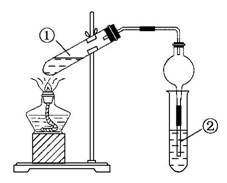
请回答下列问题:
(1)写出试管①中主要反应的化学方程式:_____________________________。
(2)加入浓硫酸的作用是________________________。
(3)试管②中观察到的现象是________________________。
(4)该实验中球形干燥管除起冷凝作用外,另一重要作用是________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com