

���� �������[��Ҫ�ɷ�ΪCu��OH��2��Ni��OH��2��Fe��OH��2��Al��OH��3��ɰ��]�������ܽ⣬���ˣ���Һ�к���Cu2+��Ni2+��Fe2+��Al3+����⣬ͭ�����������õ�������Cu����������������ʧ��������Fe3+�����ˣ���Һ�к���Ni2+��Fe3+��Al3+���ټ������ƣ�����FePO4��A1PO4���������ˣ���Һ�к���Ni2+����Һ�����л���ȡ����ȡ����Һ���л����м����ᣬ��Һ��ˮ����ΪNiSO4��
��1������Ӱ�����ʵ����ط�����
��2��ͭ�����������õ��ӣ�������Fe2+ʧ��������Fe3+��
��3�������Ӧ�ÿ�����Һ��PO43-��ʹFe3+��Al3+ȫ��ת��Ϊ��������Ni2+�����ɳ���������Ksp���㣻
��4����֪����ƽ�⣺NiSO4��ˮ�㣩+2��HA��2���л��㣩?Ni��HA2��2���л��㣩+H2SO4��ˮ�㣩������Ӧ���Ũ�ȣ�ƽ�������ƶ���
��5������ʹƽ�������ƶ����������������Ũ�ȣ�
��6��������ȡNiSO4�IJ���ܺ͢ݷ�����
��� �⣺�������[��Ҫ�ɷ�ΪCu��OH��2��Ni��OH��2��Fe��OH��2��Al��OH��3��ɰ��]�������ܽ⣬���ˣ���Һ�к���Cu2+��Ni2+��Fe2+��Al3+����⣬ͭ�����������õ�������Cu����������������ʧ��������Fe3+�����ˣ���Һ�к���Ni2+��Fe3+��Al3+���ټ������ƣ�����FePO4��A1PO4���������ˣ���Һ�к���Ni2+����Һ�����л���ȡ����ȡ����Һ���л����м����ᣬ��Һ��ˮ����ΪNiSO4��
��1���������[��Ҫ�ɷ�ΪCu��OH��2��Ni��OH��2��Fe��OH��2��Al��OH��3��ɰ��]�������ܽ⣬��Ҫ��߽������ʿ�������Ӧ���Ũ�ȣ������������Ũ�ȣ����������¶ȣ�
�ʴ�Ϊ��ad��
��2��ͭ�����������õ�������Cu������������ͭ�����������ɣ�������ͭ�����������õ�������Cu��������Fe2+ʧ��������Fe3+�����ⷽ��ʽΪ��Cu2++2Fe2+$\frac{\underline{\;ͨ��\;}}{\;}$Cu+2Fe3+��
�ʴ�Ϊ��������Cu2++2Fe2+$\frac{\underline{\;ͨ��\;}}{\;}$Cu+2Fe3+��
��3�������Ӧ�ÿ�����Һ��PO43-��ʹFe3+��Al3+ȫ��ת��Ϊ��������Ni2+�����ɳ�����
��û��Ni3��PO4��2�������ɣ���Ksp[Ni3��PO4��2]=c3��Ni2+����c2��PO43-��=��0.1��3��c2��PO43-��=4.0��10-31������c��PO43-��=2.0��10-14mol/L��
��ʹFe3+��Al3+ȫ��ת��Ϊ������FePO4��KspС�ȳ�����Al3+��ȫ����ʱFe3+Ҳ��ȫ������
Ksp[AlPO4]=c��Al3+����c��PO43-��=��1O-5����c��PO43-��=1.0��l0-19������c��PO43-��=1.0��10-14mol/L������c��PO43-��=1.0��10-14mol/LʱFe3+��Al3+ȫ��ת��Ϊ������
������Һ��c��PO43-���ķ�ΧΪ��1.0��l0-14��2.0��10-14��
�ʴ�Ϊ��1.0��l0-14��2.0��10-14��
��4����֪����ƽ�⣺NiSO4��ˮ�㣩+2��HA��2���л��㣩?Ni��HA2��2���л��㣩+H2SO4��ˮ�㣩������Ӧ���Ũ�ȣ�ƽ�������ƶ�������Ϊ��ʹ����ƽ��������Ӧ�����ƶ�Ӧ�ü����л���ȡ����
�ʴ�Ϊ�������л���ȡ����
��5�����������Ϊ����ȡ������ƽ�⣺NiSO4��ˮ�㣩+2��HA��2���л��㣩?Ni��HA2��2���л��㣩+H2SO4��ˮ�㣩�����ƶ����������������Ũ�ȣ����Լ������ᷴ��ȡ����
�ʴ�Ϊ�����
��6��������м��л���ȡ������Һ��ˮ���к������ᣬ������м�������Ϊ����ȡ������Һ�л���Ϊ�л���ȡ������������л���ȡ������ѭ��ʹ�ã�
�ʴ�Ϊ��������л���ȡ����
���� ���⿼�������ʵķ��롢�ᴿ�ķ���ѡ��Ӧ�ã��Ѷ��еȣ���ȷ�����ʵ������ǽⱾ��Ĺؼ���ע����������ᴿ�������Լ�ƽ���ƶ�ԭ����Ӧ�ã������ڿ���ѧ���ķ��������ͶԻ���֪ʶ���ۺ�Ӧ��������



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
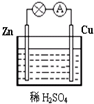 ��1��Zn��Ϊԭ��صĸ�������������������ü��ĵ缫��Ӧʽ��Zn-2e-=Zn2+������������Ӧ���������Ӧ����ԭ��Ӧ������Cu���ĵ缫��Ӧʽ��2H++2e-=H2����
��1��Zn��Ϊԭ��صĸ�������������������ü��ĵ缫��Ӧʽ��Zn-2e-=Zn2+������������Ӧ���������Ӧ����ԭ��Ӧ������Cu���ĵ缫��Ӧʽ��2H++2e-=H2�����鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ��1��NF3������Nԭ�ӵ��ӻ��������Ϊsp3���÷��ӵĿռ乹��Ϊ������
��1��NF3������Nԭ�ӵ��ӻ��������Ϊsp3���÷��ӵĿռ乹��Ϊ�������鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| ������ | Fe��OH��3 | Fe��OH��2 | Co��OH��2 | Al��OH��3 | Mn��OH��2 |
| ��ȫ������pH | 3.7 | 9.6 | 9.2 | 5.2 | 9.8 |

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

| ���� | Fe��OH��3 | Fe��OH��2 | Zn��OH��2 | Mn��OH��2/Mn��OH��3 |
| ��ʼ����pH | 2.7 | 7.6 | 5.7 | 8.3 |
| ��ȫ����pH ��c��1.0��10-5mol/L�� | 3.7 | 9.6 | 8.0 | 8.8 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
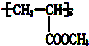 �����ִ��Ľṹ��ʽΪ��������
�����ִ��Ľṹ��ʽΪ��������| A�� | CH2�TCHCH2OH | B�� | CH3CH2OH | C�� | CH3CH��OH��CH2OH | D�� | CH2ClCHClCH2OH |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ��
���鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com