
【题目】如图是一套制取并验证氯气部分化学性质的实验装置。
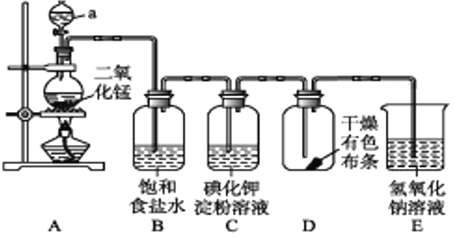
回答下列问题:
(1)装置A中,仪器a的名称叫____,该仪器中盛放的试剂为______;
(2)装置B的作用是__________________________________;
(3)当有少量Cl2通过后,观察到装置C中溶液颜色变成________色;
(4)当Cl2持续通过时,装置D中干燥的有色布条能否褪色?为什么? ________________;(5)若要证明Cl2无漂白性,则必须在装置D之前加一个装有_______的洗气瓶;
(6)装置E的作用是________,该反应的离子方程式为___________。
【答案】 分液漏斗 浓盐酸 吸收HCl 蓝 能褪色,因为Cl2与带出的H2O(g)反应生成HClO,使有色布条褪色 浓硫酸 除去多余的Cl2 Cl2+2OH-Cl-+ClO-+H2O
【解析】(1)分析装置图和仪器,装置A是氯气的发生装置,利用分液漏斗将浓盐酸滴入烧瓶中加热反应,故仪器a的名称叫分液漏斗,该仪器中盛放的试剂为浓盐酸;(2)浓盐酸易挥发,反应生成的氯气中含有氯化氢气体,利用装置B中的饱和食盐水吸收吸收HCl;(3)装置C中通过氯气会发生氧化还原反应,氯气氧化碘离子为碘单质:Cl2+2I -=2Cl-+I2,碘单质遇到淀粉变蓝;(4)当Cl2持续通过时,装置D中干燥的有色布条能褪色,因为D中虽然是干燥的有色布条,但氯气通过B、C后氯气不是干燥的,因为Cl2与带出的H2O(g)反应生成HClO,使有色布条褪色;5)若要证明Cl2无漂白性,则必须在装置D之前加一个装有浓硫酸的洗气瓶,将氯气干燥;(6)装置E的作用是除去多余的Cl2,以免直接排放到空气中造成污染,反应的离子方程式为:Cl2+2OH-Cl-+ClO-+H2O。


科目:高中化学 来源: 题型:
【题目】下列物质的分类采用树状分类法的是( )
A. 铁是单质又是导体
B. 纯净物可分为有机物和无机物
C. 氯化钠是钠的化合物,又是氯化物
D. 氢氧化钙既是纯净物,又是化合物,属于碱
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】H2O2被称为绿色氧化剂,受到人们越来越多的关注。为比较Fe3+和Cu2+对H2O2分解的催化效果,某化学研究小组的同学分别设计了如图甲、乙所示的实验。请问答下列问题:
(1)定性分析:图甲可通过观察____________,定性比较得出结论。有同学提出将FeCl3溶液改为Fe2(SO4)3溶液更合理,其理由是_____________。

(2)定量分析:如图乙所示,实验时均以生成40mL气体为准,其他可能影响实验的因素均已忽略。图中仪器A的名称为_________,检查该装置气密性的方法是:关闭分液漏斗的活塞,将注射器活塞向外拉出一段后松手,过一段时间后看________,实验中需要测量的数据是_______。

(3)课本在研究浓度对反应速率影响的实验中,酸性高锰酸钾和草酸反应的离子方程式为________,反应开始一段时间后反应速率明显提升的原因是____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】药物是人类抵御疾病的重要武器之一。下列有关药物的说法不正确的是
A.盘尼西林是一种良效广谱抗生素B.阿司匹林是一种重要的抗生素
C.青霉素是最重要的抗生素D.鸦片、吗啡、海洛因都属于毒品
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】主族元素A、B、C、D的原子序数依次增加。甲、丙、戊是由这些元素组成的二元化合物,丙分子中原子个数比为1:1,乙是元素D的单质,通常为深红棕色液体,丁为淡黄色固体,0.01 mol/L戊溶液的pH为2,己为难溶于水、密度比水大的油状物。上述物质的转化关系如图所示。下列说法中不正确的是

A. 四种元素既不同周期也不同主族
B. 元素的非金属性A<B<C
C. 丙常温常压下为气态
D. C的最高价氧化物对应的水化物为强酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】《新科学家》网站报道,科学家通过电解Fe2O3、SiO2、CaO的熔融液(1 600 ℃)制得了铁,按照树状分类法对熔融液中的三种物质进行分类,其中正确的是( )
A. 都属于混合物B. 都属于金属氧化物
C. 都属于纯净物D. 都属于非金属氧化物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有1﹣20号元素A、B、C、D所对应的物质的性质或微粒结构如下:
①A的原子M层上有6个电子;
②B2+与D﹣具有相同的电子层结构,且可以相互组合形成常见干燥剂;
③元素C的单质常温为双原子气体分子,其氢化物水溶液呈碱性;
④元素D的最高正化合价为+7价.请回答下列问题:
(1)B的离子与D的离子相互组合形成的干燥剂的化学式是 .
(2)元素C与氢元素形成带一个单位正电荷的离子,为10电子微粒,写出该微粒的电子式(用元素符号表示) .
(3)元素A与元素D相比,非金属性较强的是(用元素符号表示),下列表述中能
证明这一事实的是 .
a.常温下A的单质和D的单质状态不同
b.D的氢化物比A的氢化物稳定
c.一定条件下D单质能从A的氢化物水溶液中置换出A单质
d.HD的酸性比HA酸性强.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com