
【题目】某硫酸工厂的酸性废水中砷(As)元素含量极高,为控制砷的排放,采用化学沉降法处理含砷废水,工艺流程如下:
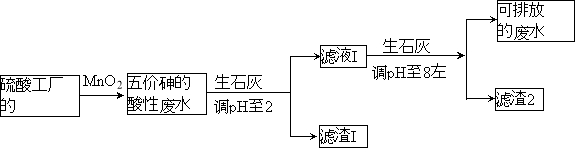
相关数据如下表,请回答以下问题:
表1.几种盐的Ksp
难溶物 | Ksp |
Ca3(AsO4)2 | 6.8×10-19 |
CaSO4 | 9.1×10-6 |
FeAsO4 | 5.7×10-21 |
表2.工厂污染物排放浓度及允许排放标准
污染物 | H2SO4 | As |
废水浓度 | 29.4g/L | 1.6g·L-1 |
排放标准 | pH 6~9 | 0.5mg·L-1 |
(1)该硫酸工厂排放的废水中硫酸的物质的量浓度c(H2SO4)= mol·L-1。
(2)若酸性废水中Fe3+的浓度为1.0×10-4mol·L-1,c(AsO43-)= mol·L-1。
(3)工厂排放出的酸性废水中的三价砷(H3AsO3弱酸)不易沉降,可投入MnO2先将其氧化成五价砷(H3AsO4弱酸),MnO2被还原为Mn2+,反应的离子方程式为 。
(4)在处理含砷废水时采用分段式,先向废水中投入生石灰调节pH到2,再投入生石灰将pH调节到8左右使五价砷以Ca3(AsO4)2形式沉降。
①将pH调节到2时废水中有大量沉淀产生,沉淀主要成分的化学式为 ;
②Ca3(AsO4)2在pH调节到8左右才开始沉淀,原因为
。
③砷酸(H3AsO4)分步电离的平衡常数(25℃)为:K1=5.6×10-3 K2=1.7×10-7 K3=4.0×10-12,第三步电离的平衡常数的表达式为K3= 。Na3AsO4的第一步水解的离子方程式为:AsO43-+H2O![]() HAsO42-+OH-,该步水解的平衡常数(25℃)为: (保留两位有效数字)。
HAsO42-+OH-,该步水解的平衡常数(25℃)为: (保留两位有效数字)。
【答案】(17分)
(1)0.3 (2分)
(2)5.7×10-17(2分)
(3)2H++MnO2+H3AsO3==H3AsO4+Mn2++H2O (3分)
(4)①CaSO4 (2分)
②H3AsO4是弱酸,当溶液中pH调节到8左右,c(AsO43-)增大,Ca3(AsO4)2开始沉淀(3分)[或:pH增大,促进H3AsO4电离,c(AsO43-)增大,Qc=c3(Ca2+)·c2(AsO43-)≥Ksp[Ca3(AsO4)2,Ca3(AsO4)2才沉淀]
③![]() (2分) 2.5×10-3(3分)
(2分) 2.5×10-3(3分)
【解析】
试题分析:(1)读表2中信息,以1L废水为研究对象,其中含有29.4gH2SO4,由于硫酸的相对分子质量为98,m/M=n,则n(H2SO4)=29.4g÷98g/mol=0.3mol,由于c=n/V,则c(H2SO4)=0.3mol÷1L=0.3mol/L;(2)FeAsO4是难溶盐,废水中存在其沉淀溶解平衡:FeAsO4 (s)![]() Fe3++AsO43-,则Ksp(FeAsO4)=c(Fe3+)c(AsO43-),所以c(AsO43-)= Ksp(FeAsO4)/c(Fe3+)=5.7×10-21/1.0×10-4 mol·L-1=5.7×10-17 mol·L-1;(3)H3AsO3失去2个电子被氧化为H3AsO4,MnO2得到2个电子被还原为Mn2+,废水是酸性溶液,根据电子、电荷、原子守恒原理可得:2H++MnO2+H3AsO3==H3AsO4+Mn2++H2O;(4)①由于CaO+2H+==Ca2++H2O,读表1中信息可知,加入生石灰调解pH到2时,增大钙离子浓度,使CaSO4 (s)
Fe3++AsO43-,则Ksp(FeAsO4)=c(Fe3+)c(AsO43-),所以c(AsO43-)= Ksp(FeAsO4)/c(Fe3+)=5.7×10-21/1.0×10-4 mol·L-1=5.7×10-17 mol·L-1;(3)H3AsO3失去2个电子被氧化为H3AsO4,MnO2得到2个电子被还原为Mn2+,废水是酸性溶液,根据电子、电荷、原子守恒原理可得:2H++MnO2+H3AsO3==H3AsO4+Mn2++H2O;(4)①由于CaO+2H+==Ca2++H2O,读表1中信息可知,加入生石灰调解pH到2时,增大钙离子浓度,使CaSO4 (s)![]() Ca2++SO42-的平衡向左移动,析出CaSO4沉淀[加入生石灰调解pH到2时,增大钙离子浓度,使Qc=c(Ca2+)·c(SO42-)≥Ksp[CaSO4),开始析出CaSO4沉淀];②H3AsO4是弱酸,当溶液中pH调节到8左右,c(AsO43-)增大,Ca3(AsO4)2 (s)
Ca2++SO42-的平衡向左移动,析出CaSO4沉淀[加入生石灰调解pH到2时,增大钙离子浓度,使Qc=c(Ca2+)·c(SO42-)≥Ksp[CaSO4),开始析出CaSO4沉淀];②H3AsO4是弱酸,当溶液中pH调节到8左右,c(AsO43-)增大,Ca3(AsO4)2 (s) ![]() 3Ca2++2AsO43-的平衡向左移动,开始析出Ca3(AsO4)2沉淀[或pH增大,促进H3AsO4电离,c(AsO43-)增大,Qc=c3(Ca2+)·c2(AsO43-)≥Ksp[Ca3(AsO4)2,Ca3(AsO4)2才沉淀];③多元弱酸分步电离,则H3AsO4
3Ca2++2AsO43-的平衡向左移动,开始析出Ca3(AsO4)2沉淀[或pH增大,促进H3AsO4电离,c(AsO43-)增大,Qc=c3(Ca2+)·c2(AsO43-)≥Ksp[Ca3(AsO4)2,Ca3(AsO4)2才沉淀];③多元弱酸分步电离,则H3AsO4![]() H++H2AsO4-、H2AsO4-
H++H2AsO4-、H2AsO4-![]() H++HAsO42-、HAsO42-
H++HAsO42-、HAsO42-![]() H++AsO43-,根据平衡常数定义式可得,第三步电离平衡常数K3=[ c(H+) c(AsO43-)]/ c(HAsO42-);水的离子积常数Kw= c(H+) c(OH-),AsO43-+H2O
H++AsO43-,根据平衡常数定义式可得,第三步电离平衡常数K3=[ c(H+) c(AsO43-)]/ c(HAsO42-);水的离子积常数Kw= c(H+) c(OH-),AsO43-+H2O![]() HAsO42-+OH-的平衡常数的计算表达式为[c(HAsO42-)c(OH-)]/ c(AsO43-),分子、分母同时乘以c(H+),则水解平衡常数=[c(HAsO42-)c(OH-) c(H+)]/[ c(H+)c(AsO43-)]= Kw/K3=(1.0×10-14)÷(4.0×10-12)=2.5×10-3。
HAsO42-+OH-的平衡常数的计算表达式为[c(HAsO42-)c(OH-)]/ c(AsO43-),分子、分母同时乘以c(H+),则水解平衡常数=[c(HAsO42-)c(OH-) c(H+)]/[ c(H+)c(AsO43-)]= Kw/K3=(1.0×10-14)÷(4.0×10-12)=2.5×10-3。


科目:高中化学 来源: 题型:
【题目】下图是利用废铜屑(含杂质)制备胆矾(硫酸铜晶体)的过程
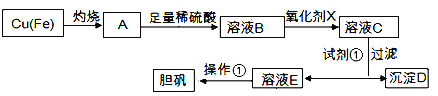
已知:
溶液中被沉淀的离子 | Fe3+ | Fe2+ | Cu2+ |
完全生成氢氧化物的沉淀时,溶液的pH | ≥3.7 | ≥6.4 | ≥4.4 |
请回答:
(1)下列物质中最适宜做氧化剂X的是________(填字母)。
A. NaClO B. H2O2 C.KMnO4
(2)加入试剂①是为了调节pH,试剂①可以选择________(填化学式)。
(3)操作①的名称是________。
(4)沉淀D加入盐酸可以得到FeCl3溶液,关于FeCl3溶液的性质中说法不正确的是________。
A. 将FeCl3饱和溶液逐滴加入沸水中,并继续加热得到红褐色液体,该液体能产生丁达尔效应
B. 向FeCl3溶液滴加NaOH溶液,出现红褐色沉淀
C. 将FeCl3溶液滴加NaOH溶液,将沉淀干燥灼烧,得到Fe(OH)3固体
D. 向FeCl3溶液中滴加KSCN溶液,溶液变为红色
(5) 沉淀D加入盐酸和铁粉,可以制得FeCl2溶液,实验室保存FeCl2溶液,需加入过量的铁粉防止FeCl2溶液变质,其原因是________________(用离子方程式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】绿矾是含有一定量结晶水的硫酸亚铁(FeSO4·XH2O),在工农业生产中具有重要的用途。某化学兴趣小组对绿矾的一些性质进行探究。回答下列问题:
(1)在试管中加入少量绿矾样品,加水溶解,滴加KSCN溶液,溶液颜色无明显变化。再向试管中通入空气,溶液逐渐变红。由此可知:______________、_______________。
(2)为测定绿矾中结晶水含量,将石英玻璃管(带两端开关K1和K2)(设为装置A)称重,记为m1 g。将样品装入石英玻璃管中,再次将装置A称重,记为 m2 g。按下图连接好装置进行实验。
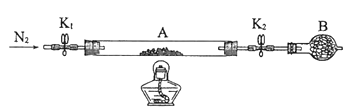
①仪器B的名称是____________________。
②将下列实验操作步骤正确排序___________________(填标号);重复上述操作步骤,直至A恒重,记为m3 g。
a.点燃酒精灯,加热 b.熄灭酒精灯 c.关闭K1和K2
d.打开K1和K2,缓缓通入N2 e.称量A f.冷却至室温
③根据实验记录,计算绿矾化学式中结晶水数目x=________________(列式表示)。若实验时按a、d次序操作,则使x__________(填“偏大”“偏小”或“无影响”)。
(3)为探究硫酸亚铁的分解产物,将(2)中已恒重的装置A接入下图所示的装置中,打开K1和K2,缓缓通入N2,加热。实验后反应管中残留固体为红色粉末。C、D中的溶液依次为BaCl2溶液、浓H2SO4。C、D中有气泡冒出,并可观察到的现象分别为产生白色沉淀、品红溶液褪色。写出硫酸亚铁高温分解反应的化学方程式_____________________。
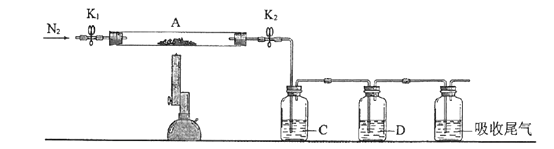
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组变化中,化学反应的反应热前者大于后者的一组是( )
①CH4(g)+2O2(g)=CO2(g)+2H2O(g)△H1;
CH4(g)+2O2(g)=CO2(g)+2H2O(l)△H2;
②2H2(g)+O2(g)=2H2O(l)△H1;
H2(g)+O2(g)=H2O(l)△H2
③t℃时,在一定条件下,将1molSO2和1molO2分别置于恒容和恒压的两个密闭容器中,达到平衡状态时放出的热量分别为Q1、Q2
④CaCO3(s)=CaO(s)+CO2(g)△H1;
CaO(s)+H2O(l)=Ca(OH)2(s)△H2
A. ③④ B. ②③ C. ①② D. ①④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铁矿石主要成分为铁的氧化物(设杂质中不含铁元素和氧元素,且杂质不与H2SO4反应)。有一种测定铁矿石中含铁量的方法如下。已知:2Na2S2O3+I2→Na2S4O6+2NaI。完成下列填空:
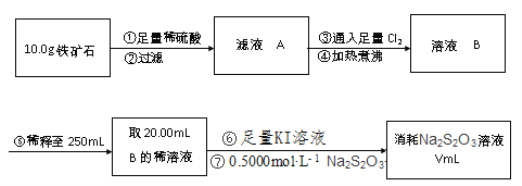
(1)步骤②用到的玻璃仪器除烧杯外,还有______。
(2)步骤③对应反应的离子方程式为______。
(3)步骤④中煮沸的作用是______。步骤⑤中必须用到的定量实验仪器是______。
(4)步骤⑦可用淀粉作为滴定终点的指示剂,达到滴定终点时的现象是______。若滴定过程中有空气进入,则测定结果______(选填“偏高”、“偏低”或“无影响”。
(5)若过程⑦中消耗0.5000mol/LNa2S2O3溶液20.00mL,则铁矿石中铁的百分含量为______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某氯化钾样品中含有少量碳酸钾、硫酸钾和不溶于水的杂质。为了提纯氯化钾,先将样品溶于适量水中,充分搅拌后过滤,再将滤液按如图所示步骤进行操作。下列说法中正确的是
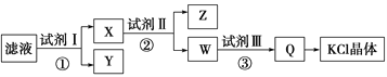
A. 起始滤液的pH=7
B. 试剂Ⅰ为Ba(NO3)2溶液
C. 步骤②中加入试剂Ⅱ的目的是除去Ba2+
D. 图示的步骤中必须要经过2次过滤操作
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某校化学兴趣小组的同学分别对氯气和氯水的性质进行探究。
Ⅰ.下图是实验室制备氯气并进行一系列相关实验的装置(部分夹持装置已略)。
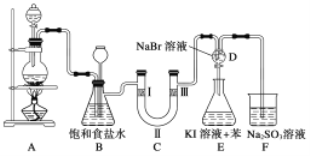
(1)制备氯气选用的药品为二氧化锰和浓盐酸,A中反应的化学方程式为
__________________________________。
(2)装置B中饱和食盐水的作用是______;同时装置B还能监测实验进行时C中是否发生堵塞,请写出发生堵塞时B中的现象______。
(3)装置C的实验目的是验证氯气是否具有漂白性,为此C中Ⅰ、Ⅱ、Ⅲ处最好依次放入________(填序号)。
①干燥的有色布条 ②湿润的有色布条 ③碱石灰④无水氯化钙 ⑤浓硫酸
(4)当向D中缓缓通入一定量氯气时,D中溶液逐渐变为______色;再打开D装置活塞,将装置D中少量溶液滴入锥形瓶E中,振荡,观察到的现象是___________________。
(5)有人提出,装置F中可改用足量的饱和NaHSO3溶液吸收氯气,请判断是否可行________(填“是”或“否”),理由是__________________________________ (用离子反应方程式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,将Cl2缓慢通入水中。当通入的Cl2体积为V1时达到饱和,溶液中c(H+)变化如下图中曲线a。已知Cl2的溶解度随温度升高而迅速降低,下列叙述中正确的是
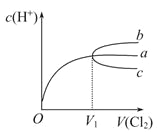
A. 将饱和氯水升温,继续通入Cl2时,溶液中c(H+)变化如曲线b
B. 在饱和氯水中通入SO2气体,溶液中c(H+)变化如曲线c
C. 降温,继续通入Cl2时,溶液中c(H+)增大
D. 在饱和氯水中加入NaOH使pH=7,所得溶液中存在下列关系c(Na+)>c(ClO-)>c(Cl-)>c(HClO)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某研究性学习小组设计了如图装置制取和验证SO2的性质。
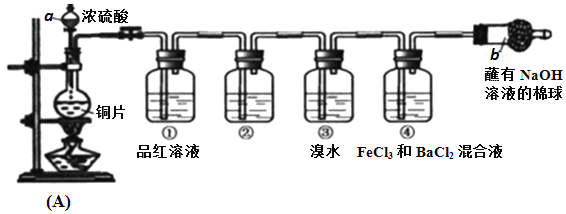
请回答:
(1)写出A反应装置中的化学方程式:____________
(2)棉球中NaOH溶液的作用是________________
(3)为了验证SO2是酸性氧化物,洗气瓶②中可选择的试剂是_________。
A.澄清石灰水 B.无色酚酞试液 C.碘水 D.紫色石蕊试液
(4)下列说法正确的是____________。
A.先向装置中加入试剂(药品),再进行气密性检查
B.实验开始时,只需打开分液漏斗的旋塞,即可使液体顺利滴下
C.实验开始后,洗气瓶①和③中溶液均褪色,两者均可证明SO2具有漂白性
D.实验开始后,洗气瓶④中可观察到白色沉淀产生,该现象可说明SO2具有还原性
(5)写出洗气瓶③中反应的化学方程式:_____________
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com