
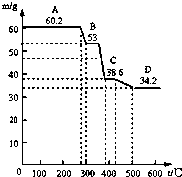
 ijУ�о���ѧϰС��ȡ���������ƺŵ�ˮ��ʯ��Ʒ�����̽������ش�������⣮
ijУ�о���ѧϰС��ȡ���������ƺŵ�ˮ��ʯ��Ʒ�����̽������ش�������⣮| (60.2-53)g |
| 18g/mol |
| 38.6g-34.2g |
| 44g/mol |
| 3 |
| 2 |
| c |
| 2 |
| 2a+3b |
| d |
| 18 |
| 1 |



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
A�� |
| B��H2SO4 |
C�� |
D�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A����3���ڢ�B�� |
| B����4���ڢ�B�� |
| C����4���ڢ��� |
| D����4���ڢ�A�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��-1 | B��+2 | C��+3 | D��0 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��7.8g Na2O2���е���������ĿΪ0.2NA |
| B��PH=2�Ĵ����ϡ10������Һ��H+��Ŀ����0.001NA |
| C��25��ʱ��1.0L pH=9��CH3COONa��Һ��H+��CH3COOH������ĿΪ10-5NA |
| D����֪�Ȼ�ѧ����ʽ2SO2��g��+O2��g��?2SO3��g����H=-Q kJ?mol-1 ��Q��0������2NA ��SO2���Ӻ�NA ��O2����������һ�ܱ������г�ַ�Ӧ��ų�QkJ�� ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A����������ϡ���ᷴӦ��1 mol Feʧȥ������Ϊ3NA |
| B�����³�ѹ�£�22.4L ��ϩ�к����Թ��ۼ���ĿΪ5NA |
| C��1 mol Cu������Ũ���ᷴӦ����2NA��SO2���� |
| D��1 mol�������1 mol�Ҵ���Ũ��������³�ַ�Ӧ����H2O����ΪNA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com