
| A. | 将0.1molCl2全部溶于水形成的1L溶液中:2c(Cl2)+c(Cl-)+c(HClO)+c(ClO-)=0.2mol•L-1 | |
| B. | Na2CO3溶液中:c(OH-)-c(H+)=c(HCO3-)+c(H2CO3) | |
| C. | 物质的量浓度均为0.1mol•L-1的NaClO与NaHCO3的混合溶液中:c(HClO)+c(ClO-)=c(HCO3-)+c(H2CO3)+c(CO32-) | |
| D. | 室温下,向0.01mol•L-1的NH4HSO4溶液中滴加NaOH溶液至中性:c(Na+)>c(SO42-)>c(NH4+)>c(OH-)=c(H+) |
分析 A.氯元素守恒分析微粒守恒关系;
B.碳酸钠溶液中存在质子守恒,水电离出所有氢离子浓度等于其电离出的所有氢氧根离子浓度;
C.物质的量浓度均为0.1mol•L-1的NaClO与NaHCO3的混合溶液中存在物料守恒,n(Cl)=n(C);
D.向 NH4HSO4中滴加NaOH溶液,当二者物质的量相同时,溶质为等物质的量的(NH4)2SO4和Na2SO4,溶液呈酸性,再滴加少许NaOH呈中性.
解答 解:A.将0.1molCl2全部溶于水形成的1L溶液中氯元素物质的量浓度总和为0.2mol/L,2c(Cl2)+c(Cl-)+c(HClO)+c(ClO-)=0.2mol•L-1 ,故A正确;
B.Na2CO3溶液中存在质子守恒:c(OH-)-c(H+)=c(HCO3-)+2c(H2CO3),故B错误;
C.物质的量浓度均为0.1mol•L-1的NaClO与NaHCO3的混合溶液中存在物料守恒:c(HClO)+c(ClO-)=c(HCO3-)+c(H2CO3)+c(CO32-),故C正确;
D.向 NH4HSO4中滴加NaOH溶液,当二者物质的量相同时,溶质为等物质的量的(NH4)2SO 4和Na2SO 4,溶液呈酸性,再滴加少许NaOH呈中性,c(Na+)>c(SO42-)>c(NH4+)>c(OH-)=c(H+),故D正确;
故选B.
点评 本题考查了溶液中物料守恒分析、离子浓度大小比较、注意元素的所有存在形式的判断,掌握基础是解题关键,题目难度中等.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:选择题
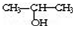 与NaOH的醇溶液共热制备CH3-CH═CH2
与NaOH的醇溶液共热制备CH3-CH═CH2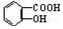 与适量NaHCO3溶液反应制备
与适量NaHCO3溶液反应制备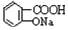
| A. | 只有③④ | B. | 只有①④ | C. | 只有① | D. | 都不能 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 实验室应将钠保存在煤油中 | |
| B. | 分液漏斗和容量瓶在使用前都要检漏 | |
| C. | 可用酒精代替CCl4萃取碘水中的碘单质 | |
| D. | 金属镁失火不可用水来灭火 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 干冰和石英晶体中的化学键类型相同,熔化时需克服微粒间的作用力类型也相同 | |
| B. | 化学变化发生时,需要断开反应物中的化学键,并形成生成物中的化学键 | |
| C. | CH4和CCl4中,每个原子的最外层都具有8电子稳定结构 | |
| D. | NaHSO4晶体溶于水时,离子键被破坏,共价键不受影响 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
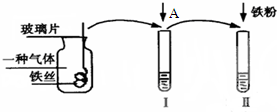 如图是某次实验探究铁及其化合物性质的流程图:
如图是某次实验探究铁及其化合物性质的流程图:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 让Cl2和H2混合后,点燃生成氯化氢气体,再将氯化氢气体通入水中获得盐酸 | |
| B. | 制备硫酸,用水吸收三氧化硫气体生成浓硫酸 | |
| C. | 侯氏制碱法,将二氧化碳通入含氨的氯化钠饱和溶液中,过滤得到碳酸氢钠晶体 | |
| D. | 用电解熔融氯化铝和冰晶石的混合物的方法得到铝 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com