
废电池必须进行集中处理的问题被提到议事日程,其首要原因是
A.利用电池外壳的金属材料
B.回收其中的石墨电极
C.防止电池中的汞、镉和铅等重金属离子对土壤和水的污染
D.不使电池中渗泄的电解液腐蚀其它物
科目:高中化学 来源: 题型:
下列事实中,不能说明氯的非金属性比硫强的是
A.氯化氢比硫化氢的热稳定性好
B.次氯酸的氧化性比稀硫酸强
C.氯气通入硫化钠溶液出现淡黄色浑浊
D.化合物SCl2中硫显正化合价而氯为负价
查看答案和解析>>
科目:高中化学 来源: 题型:
设阿伏加德罗常数为NA,标准状况下,m g N2和O2的混合气体含有b个分子,则n g该混合气体在相同状态下的体积为(单位为L)( )
A. B.
B.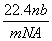
C. D.
D.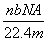
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是
A.“钡餐”中使用的硫酸钡是弱电解质
B.太阳能电池板中的硅在周期表中处于金属与非金属的交界位置
C.常用的自来水消毒剂有Cl2和二氧化氯,两者都含极性键
D.“滴水穿石”不涉及化学变化
查看答案和解析>>
科目:高中化学 来源: 题型:
在密闭容器中进行反应:2A+3B 2C。开始时C的浓度为amol·L-1,2min后C的浓度变为2amol·L-1,A和B的物质的量浓度均变为原来的1/2,则下列说法中不正确的是
2C。开始时C的浓度为amol·L-1,2min后C的浓度变为2amol·L-1,A和B的物质的量浓度均变为原来的1/2,则下列说法中不正确的是
A.用B表示的反应速率是0.75a mol/(L·min)
B.反应开始时,c(B)=3amol·L-1
C.反应2min后,c(A)=0.5amol·L-1
D.反应2min后,c(B)=1.5amol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
下列条件一定能使化学反应速率增大的是
①增加反应物的量 ②升高温度 ③缩小反应容器的体积 ④加入生成物
A.只有② B.只有②③ C.只有①② D.全部
查看答案和解析>>
科目:高中化学 来源: 题型:

(1)合成氨工业对国民经济和社会发展具有重要的 意义。某合成氨工业中氢气由天然气和水反应制备,其主要反应为:
CH4 (g)+ 2H2O (g)  CO2(g)+4H2 (g)
CO2(g)+4H2 (g)
反应过程中能量变化如图所示,则该反应为__________反应(填“吸热”或“放热”)
(2)某温度下,10L密闭容器中充入2mol CH4和 3molH2O(g),发生CH4 (g)+ 2H2O (g)  CO2(g)+4H2 (g)反应,反应进行到4s时CO2 的物质的量浓度为0.08mol/L,再过一段时间反应达平衡,平衡时容器的压强是起始时的1.4倍。则:
CO2(g)+4H2 (g)反应,反应进行到4s时CO2 的物质的量浓度为0.08mol/L,再过一段时间反应达平衡,平衡时容器的压强是起始时的1.4倍。则:
①前4s以CH4浓度变化表示的平均反应速率为多少?
② 4s时,混合气体中H2的体积分数为多少?
③平衡时,H2O (g)的浓度是多少?(要求:写出计算过程)
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于能源和作为能源物质的叙述中不正确的是( )
A.人类利用的能源都是通过化学反应获得的
B.绿色植物进行光合作用时,将太阳能转化为化学能“贮存”起来
C.物质的化学能可以在不同条件下转为热能、电能为人类所利用
D.化石燃料蕴藏的能量来自远古时期生物体所吸收利用的太阳能
查看答案和解析>>
科目:高中化学 来源: 题型:
降低大气中CO2的含量及有效地开发利用 CO2,目前工业上有一种方法是用CO2来生产甲醇燃料。为探究反应原理,现进行如下实验,在体积为1L的恒容密闭容器中,充入1mol CO2和3mol H2,一定条件下发生反应:CO2(g)+3H2(g) CH3OH(g)+H2O(g) ΔH =-49.0kJ/mol。测得CO2和CH3OH(g)的浓度随时间变化如图所示。
CH3OH(g)+H2O(g) ΔH =-49.0kJ/mol。测得CO2和CH3OH(g)的浓度随时间变化如图所示。
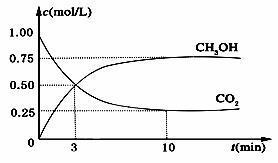
(1)从反应开始到平衡,氢气的平均反应速率v(H2)=________mol/(L·min);
(2)氢气的转化率=________;
(3)该反应的平衡常数为________(保留小数点后2位);
(4)下列措施中能使平衡体系中n(CH3OH)/n(CO2)增大的是________。
A.升高温度
B.充入He(g),使体系压强增大
C.将H2O(g)从体系中分离出去
D.再充入1mol H2
(5)当反应达到平衡时,H2的物质的量浓度为c1,然后向容器中再加入一定量H2,待反应再一次达到平衡后,H2的物质的量浓度为c2,则c1________c2的关系(填“>”、“<”或“=”)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com