
| A、硫酸氢钠和氢氧化钡 |
| B、氢氧化钾和盐酸 |
| C、硝酸和氢氧化钠 |
| D、氢氧化钡和硝酸 |


科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
| A、K+、Fe3+、CO32-、NO3- |
| B、H+、K+、MnO4-、Cl- |
| C、Ba2+、Na+、HCO3-、OH- |
| D、K+、Na+、SO42-、S2- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Ba(OH)2溶液与稀H2SO4混合:2H++2OH-=2H2O |
| B、氢氧化镁溶于盐酸:Mg+2OH-+2H+=Mg2++2H2O |
| C、少量铁粉加入稀硝酸中:Fe+NO3-+4H+=Fe3++NO↑+2H2O |
| D、钠放入水中:Na+H2O=Na++OH-+H2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、35Cl2与37Cl2互为同位素 |
B、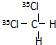 和 和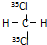 互为同分异构体 互为同分异构体 |
| C、与37Cl的得电子能力相同 |
| D、35Cl-和与它核外电子排布相同的微粒化学性质相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 1 |
| 2 |

| 滴定次数 | 1 | 2 | 3 | 4 |
| KMnO4溶液体积/mL | 20.60 | 20.02 | 20.00 | 29.98 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①②⑨⑩ | B、③⑤⑥⑩ |
| C、③⑥⑦⑩ | D、④⑤⑧⑩ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 选项 | 实验目的 | 实验方案 |
| A | 验证Ksp(AgCl)>Ksp(AgI) | 向NaCl溶液中滴加少量AgNO3溶液,产生白色沉淀,再滴加KI溶液,可观察到白色沉淀转化为黄色沉淀 |
| B | 检验Fe(NO3)2晶体是否已氧化变质 | 将Fe(NO3)2样品溶于稀H2SO4后,滴加KSCN溶液,观察溶液是否变红 |
| C | 验证Br2的氧化性强于I2 | 将少量溴水加入KI溶液中,再加入CCl4,振荡,静置.可观察到下层液体呈紫色 |
| D | 比较确定铜和镁的金属活动性强弱 | 用石墨作电极电解Mg(NO3)2、Cu(NO3)2的混合液 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com