
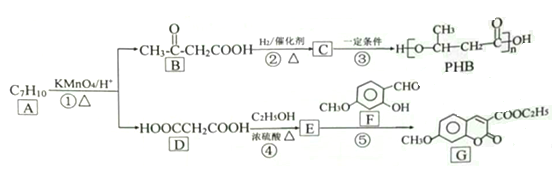
【题目】由化合物A制备一种医药合成中间体G和可降解环保塑料PHB的合成路线如下:
己知: ![]() (-R1、-R2、-R3均为烃基)
(-R1、-R2、-R3均为烃基)
回答下列问题:
(1)A的结构简式___________,G中含氧官能团的名称____________________。
(2)反应①和③的反应类型分别是_____________、________________。
(3)C存在多种同分异构体,其中分别与足量的NaHCO3溶液和Na反应产生气体的物质的量相同的同分异构体的数目为______种。
(4)写出反应③的化学方程式__________________________________
(5)写出满足下列条件的B的同分异构体_________________________
①能发生银镜反应 ②分子中烃基上的氢原子被取代后的一氯代物只有一种
(6)写出用B为起始原料制备高分子化合物![]() 的合成路线(其
的合成路线(其
他试剂任选)。____________________________________________
(7)上述合成路线中最后一步反应的化学方程式为:______________________
【答案】 ![]() 醚键、酯基 氧化反应 缩聚反应 4
醚键、酯基 氧化反应 缩聚反应 4 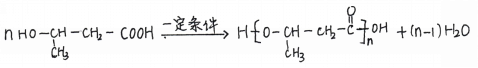
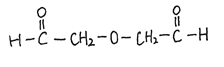

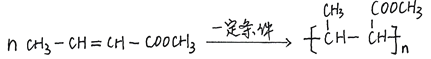
【解析】根据信息![]() 可知,A被酸性高锰酸钾氧化为CH3COCH2COOH 和HOOCCH2COOH,所以A为
可知,A被酸性高锰酸钾氧化为CH3COCH2COOH 和HOOCCH2COOH,所以A为![]() ;CH3COCHCCOOH与氢气发生加成反应生成C,结构简式为:CH3CH(OH)CH2COOH;HOOCCH2COOH与乙醇反应生成E,E为二元酯:CH3CH2OOCCH2COOCH2CH3。
;CH3COCHCCOOH与氢气发生加成反应生成C,结构简式为:CH3CH(OH)CH2COOH;HOOCCH2COOH与乙醇反应生成E,E为二元酯:CH3CH2OOCCH2COOCH2CH3。
(1)结合以上分析可知,A的结构简式![]() ;结合有机物G的结构简式,G中含氧官能团醚键、酯基;正确答案:
;结合有机物G的结构简式,G中含氧官能团醚键、酯基;正确答案: ![]() ;醚键、酯基。
;醚键、酯基。
(2)![]() 被酸性高锰酸钾溶液氧化,反应①发生氧化反应;根据PHB的结构简式可知,③发生了缩聚反应;正确答案:氧化反应;缩聚反应。
被酸性高锰酸钾溶液氧化,反应①发生氧化反应;根据PHB的结构简式可知,③发生了缩聚反应;正确答案:氧化反应;缩聚反应。
3)有机物C结构简式为CH3CH(OH)CH2COOH;其同分异构体满足条件:分别与足量的NaHCO3溶液和Na反应产生气体的物质的量相同,说明该有机物中含有一个羧基和一个羟基;具体结构如下:针对C-C-C-COOH结构,-OH在烃基上的位置有3种,针对![]() 结构,-OH在烃基上的位置有2种,因此满足条件的有机物共有5种,但是其中有一种与有机物C结构相同,因此,满足条件的有机物有4种;正确答案:4。
结构,-OH在烃基上的位置有2种,因此满足条件的有机物共有5种,但是其中有一种与有机物C结构相同,因此,满足条件的有机物有4种;正确答案:4。
(4)有机物C结构简式为CH3CH(OH)CH2COOH,在一定条件下发生缩聚反应生成高分子,化学方程式:nCH3CH(OH)CH2COOH ![]() (n-1)H2O+
(n-1)H2O+ ![]() ;正确答案:nCH3CH(OH)CH2COOH
;正确答案:nCH3CH(OH)CH2COOH ![]() (n-1)H2O+
(n-1)H2O+ ![]() 。
。
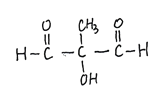
(5)有机物B为CH3COCH2COOH,其同分异构体满足条件:①能发生银镜反应,含有醛基;②分子中烃基上的氢原子被取代后的一氯代物只有一种,结构高度对称;满足下列条件的同分异构体为OHC-CH2-O-CH2-CHO 、 ![]() ;正确答案:OHC-CH2-O-CH2-CHO 、
;正确答案:OHC-CH2-O-CH2-CHO 、 ![]() 。
。
(6)根据高分子化合物![]() 可知:形成该有机物的单体为CH3-CH=CH-COOCH3;有机物B为CH3COCH2COOH,与氢气发生加成生成CH3CH(OH)CH2COOH,该有机物在浓硫酸加热条件下发生消去反应生成CH3-CH=CH-COOH;CH3-CH=CH-COOH与甲醇发生酯化生成CH3-CH=CH-COOCH3;CH3-CH=CH-COOCH3在一定条件下发生加聚反应生成高分子;合成流程如下:
可知:形成该有机物的单体为CH3-CH=CH-COOCH3;有机物B为CH3COCH2COOH,与氢气发生加成生成CH3CH(OH)CH2COOH,该有机物在浓硫酸加热条件下发生消去反应生成CH3-CH=CH-COOH;CH3-CH=CH-COOH与甲醇发生酯化生成CH3-CH=CH-COOCH3;CH3-CH=CH-COOCH3在一定条件下发生加聚反应生成高分子;合成流程如下: ;正确答案:
;正确答案: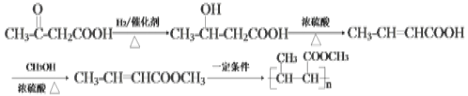 。
。
(7)上述合成路线中最后一步反应是CH3-CH=CH-COOCH3发生加聚反应生成高分子,化学方程式为:nCH3-CH=CH-COOCH3![]()
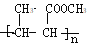 ;正确答案:nCH3-CH=CH-COOCH3
;正确答案:nCH3-CH=CH-COOCH3 ![]()
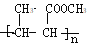 。
。


科目:高中化学 来源: 题型:
【题目】【题目】有机物E是医药合成中间体.其合成路线如图:
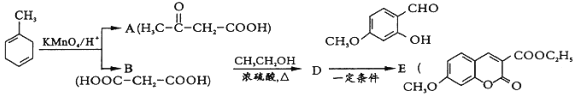
(1)![]() 的官能团名称为______.
的官能团名称为______.
(2)已知![]() 的系统命名为 2-丙酮酸,则A的名称是________________.
的系统命名为 2-丙酮酸,则A的名称是________________.
(3)D为二元酯,则B→D的化学方程式为________________________________________.
D→E的反应历程如图:

(4)写出这几步的反应类型:I_____________,Ⅱ____________III____________
(5)![]() 中能与稀 NaOH溶液反应的官能团是______.检验该官能团的方法是__________________________________________.
中能与稀 NaOH溶液反应的官能团是______.检验该官能团的方法是__________________________________________.
(6)写出满足下列条件的D的所有同分异构体的结构简式______________________________.
a.核磁共振氢谱有3组峰
b.常温下能与NaHCO3按1:2反应并释放出气体
(7)由化合物A经过两步便可以合成环境友好型高聚物聚3-羟基丁酸酯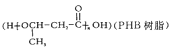
请写出反应合成线路,结合已知信息选用必要的无机试剂,用结构简式表示有机物,用箭头表示转化关系,箭头上注明试剂和反应条件_______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】金属钛(Ti)的机械强度高,抗蚀能力强,有“未来金属”之称。工业上常用硫酸浸钛铁矿(其主要成分为钛酸亚铁(FeTiO 3它难溶于水,但能与酸反应)的方法制取二氧化钛 ,再由二氧化钛 制取金属钛。工艺流程如下:

回答下列问题
(1) FeTiO3中钛元素的化合价为____。
(2)稀硫酸与FeTiO3反应的离子方程式为:____。
(3)过程V表现了金属镁的还原性比金属钛的还原性____(填“强”或“弱”)。
(4)写出过程IV的化学方程式____(注意焦炭过量)。
(5)酸浸中,铁的浸出率与时间、温度的关系如图所示,如图可知,当铁的浸出率为70%时,可采用的实验条件为____。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学设计如下微型实验装置用以验证SO2的性质,通过分析实验,下列结论表达不正确的是( )
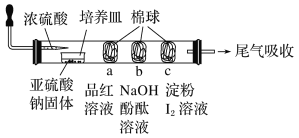
A. a棉球褪色,验证SO2具有漂白性
B. b棉球褪色,验证SO2具有酸性氧化物的性质
C. c棉球蓝色褪去,验证SO2具有还原性
D. 只能用烧碱溶液吸收尾气
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.海水晒盐后所得的苦卤中含有较高浓度的MgCl2、KCl以及金属溴化物。以下是苦卤化学分离的过程。
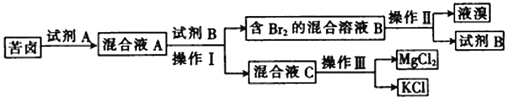
回答下列问题:
(1)若试剂A是一种有色气体单质,则A是_______(填化学式);
(2)“操作II”是_______,“操作III”是_______。(填字母)
a.蒸发 b.蒸馏 c.分液 d.重结晶
(3)试剂B可能是下列物质中的________。(填字母)
a.饱和NaCl溶液 b.CCl4 c.NaOH d.乙醇
Ⅱ.一种工业制备SrCl2·6H2O的生产流程如下图所示:

已知:①M(SrCl2·6H2O)=267g·mol-1;②Ksp(SrSO4)=3.3×10-7、Ksp(BaSO4)=1.1×10-10;③经盐酸浸取后,溶液中有Sr2+和Cl-及少量Ba2+。
(1)加入硫酸溶液的目的是______________;为了提高原料的利用率,滤液中Sr2+的浓度应不高于_________ mol·L1 (注:此时滤液中Ba2+浓度为1×105 mol·L1)。
(2)产品纯度检测:称取1.000 g产品溶解于适量水中,向其中加入含AgNO3 1.100×102 mol的AgNO3溶液(溶液中除Cl-外,不含其他与Ag+反应的离子),待Cl-完全沉淀后,用含Fe3+的溶液作指示剂,用0.2000 mol·L1的NH4SCN标准溶液滴定剩余的AgNO3,使剩余的Ag+以AgSCN白色沉淀的形式析出。
①滴定反应达到终点的现象是_________________________________________。
②若滴定过程用去上述浓度的NH4SCN溶液20.00 mL,则产品中SrCl2·6H2O的质量百分含量为_______(保留4位有效数字)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】探究电场作用下阴阳离子的迁移。a、b、c、d 均为石墨电极,电极间距4cm。将pH试纸用不同浓度Na2SO4溶液充分润湿,进行如下实验:
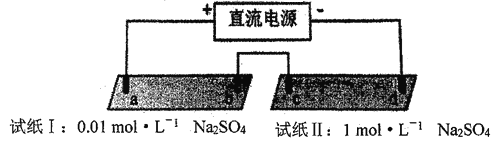
实验现象:
时间 | 试纸I | 试纸II |
lmin | a极附近试纸变红,b极附近试纸变蓝 | c极附近试纸变红,d极附近…… |
10min | 红色区和蓝色区不断向中间扩展,相遇时红色区约2.7cm,蓝色区约1.3cm | 两极颜色范围扩大不明显,试纸大部分仍为黄色 |
下列说法不正确的是
A. d极附近试纸变蓝
B. a极附近试纸变红的原因是:2H2O+2e-= H2↑+2OH-
C. 对比试纸I和试纸II的现象,说明电解质浓度环境影响H+和OH-的迁移
D. 试纸I的现象说明,此环境中H+的迁移速率比OH-快
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com