
��Ԫ�ؼ��仯�������������������ϢϢ��أ��Իش��������⣺
��1�����ӹ�ҵ����30����FeCl3��Һ��ʴ���ھ�Ե���ϵ�ͭ��������ӡˢ��·�壬�÷�Ӧ�����ӷ���ʽΪ ��
��2����֪��Fe(s)+ O2(g)
O2(g) FeO(s)
��H=��272 kJ��mol��1
FeO(s)
��H=��272 kJ��mol��1
C(s)+O2(g) CO2(g) ��H=��393.5 kJ��mol��1
CO2(g) ��H=��393.5 kJ��mol��1
2C(s)+O2(g) 2CO(g) ��H=��221 kJ��mol��1
2CO(g) ��H=��221 kJ��mol��1
���¯����������
FeO(s)+CO(g) Fe(s)+CO2(g) ��H=
��
Fe(s)+CO2(g) ��H=
��
��3�����죨Fe2O3����һ�ֺ�ɫ���ϡ���һ��������������160mL 5 mol��L��1�����У��ټ����������ۣ�����Ӧ�������ռ�������2.24L����״�������������Һ����Fe3������μӷ�Ӧ�����۵�����Ϊ ��
��4����H2��O2��������Na2CO3���ȼ�ϵ�أ����õ�ⷨ�Ʊ�Fe(OH)2��װ������ͼ��ʾ������P��ͨ��CO2��
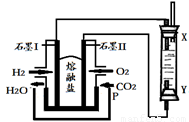
��ʯīI�缫�ϵĵ缫��ӦʽΪ ��
��ͨ��һ��ʱ����Ҳಣ�����в��������İ�ɫ�������ҽϳ�ʱ�䲻��ɫ��������˵������ȷ���� ������ţ���
A��X��Y���˶������������缫
B��������NaOH��Һ��Ϊ���Һ
C�����������ķ�Ӧ�ǣ�2H2O�� 2e��= H2��+ 2OH��
D����ɫ����ֻ���������ϲ���
����������Fe(OH)2������¶�ڿ����У�����ɫ�仯Ϊ ���÷�Ӧ�Ļ�ѧ����ʽΪ ��
��1��2Fe3��
+ Cu 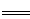 2Fe2�� + Cu2��
��2�֣�
2Fe2�� + Cu2��
��2�֣�
��2����11 kJ��mol��1 ��2�֣�
��3��11.2 g ��2�֣�
��4����H2 - 2e��+
CO32�� 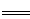 CO2+H2O��2�֣�
CO2+H2O��2�֣�
��B C ��2�֣�
�۰�ɫ����Ѹ�ٱ�ɻ���ɫ�����ձ�ɺ��ɫ��2�֣�
4Fe (OH)2��O2��2H2O��4Fe (OH)3 ��2�֣�
��������
�����������1���Ȼ�����ͭ��Ӧ�����Ȼ��������Ȼ��������ӷ���ʽΪ2Fe3�� + Cu 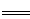 2Fe2�� + Cu2�� ��
2Fe2�� + Cu2�� ��
��2��a��Fe��s��+ O2��g���TFeO��s����H=��272 kJ��mol��1
O2��g���TFeO��s����H=��272 kJ��mol��1
b��C��s��+O2��g���TCO2��g����H=��393.5 kJ��mol��1
c��2C��s��+O2��g���T2CO��g����H=��22l kJ��mol��1
���ݸ�˹����b��c��2��a�õ���FeO��s��+CO��g��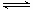 Fe��s��+CO2��g����H=��1lkJ��mol��1��
Fe��s��+CO2��g����H=��1lkJ��mol��1��
��3�����������ʵ���Ϊ 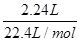 =0.1mol��
=0.1mol��
Fe �� 2HCl �� H2��
0.1mol 0.2mol 0.1mol
������ԭ���غ㣬�����Ȼ��������ʵ���Ϊ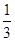 ����0.16L��5mol��L��1-0.2mol��=0.2mol��
����0.16L��5mol��L��1-0.2mol��=0.2mol��
Fe �� 2FeCl3
0.1mol 0.2mol
���Բμӷ�Ӧ�����۵�����Ϊ��0.1mol+0.1mol����56g��mol��1=11.2g��
��4����ȼ��ԭ����У�������ȼ��ʧ���Ӻ�̼������ӷ�Ӧ���ɶ�����̼��ˮ���缫��ӦʽΪH2
- 2e��+ CO32�� 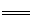 CO2+H2O��
CO2+H2O��
�ڵ�ⷨ�Ʊ�Fe (OH)2 ʱ�����ý���Fe����������������ʽΪ��Fe-2e��=Fe2�����������Ͽ�������Ҳ�������������ϣ���������ʽΪ��2H��+2e��=H2������Ϊ�����ӷŵ��ƻ�ˮ�ĵ���ƽ�⣬ʹ����������Ũ���������������ӽ�ϳ�Fe (OH)2������
����Ϊ�ڿ�����Fe (OH)2���������·�Ӧ��4Fe (OH)2��O2��2H2O��4Fe (OH)3�����ɫ�������Գ���������Fe (OH)2���ɣ���¶�ڿ����а�ɫ����Ѹ�ٱ�ɻ���ɫ�����ձ�ɺ��ɫ��
���㣺���������ۺϻ�ѧ֪ʶ��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
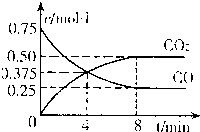 ��Ԫ�ؼ��仯�������������������ϢϢ��أ�
��Ԫ�ؼ��仯�������������������ϢϢ��أ� O2��g���TFeO��s����H=-272kJ?mol-1
O2��g���TFeO��s����H=-272kJ?mol-1�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��Ϋ��һģ ���ͣ��ʴ���
| 1 |
| 2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��Ԫ�ؼ��仯�������������������ϢϢ��أ�
������ �Իش��������⣺
����1�����ӹ�ҵ����30������FeCl3��Һ��ʴ���ھ�Ե���ϵ�ͭ��������ӡˢ��·�壬д���÷�Ӧ�����ӷ���ʽ������������������������ ��
��2����¯���������лᷢ����Ӧ��FeO��s��+CO��g����![]() �� Fe��s��+CO2��g����
�� Fe��s��+CO2��g����
��֪��Fe��s��+![]() O2��g��=FeO��s����H=-272kJ��mol-1
O2��g��=FeO��s����H=-272kJ��mol-1
C��s��+O2��g��=CO2��g�� ��H=-393��5kJ��mol-1
2C��s��+O2��g��=2CO��g���� ��H=-22lkJ��mol-1
���������� ��FeO��s��+CO��g����![]() ���� Fe��s��+CO2��g�� ��H=���������� �� ��
���� Fe��s��+CO2��g�� ��H=���������� �� ��

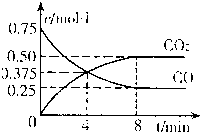
��һ���¶��£���ij�ܱ������м�������FeO��������һ������CO���壬��Ӧ������CO��CO2��Ũ����ʱ��Ĺ�ϵ��ͼ��ʾ
��ӿ�ʼ���ﵽƽ������У�![]() ��CO��=������������������������������ ���£�
��CO��=������������������������������ ���£�
FeO��s��+CO��g��![]() ���� Fe��s��+CO2��g��
���� Fe��s��+CO2��g��
�Ļ�ѧƽ�ⳣ��K=���������� ��
�� ��3��������һ�ֺ�ɫ���ϣ���ɷ���Fe2O3����һ��������������160mL5mol��L-1�����У��ټ���һ��������ǡ����ȫ�ܽ⣬�ռ�������2��24L����״����������⣬��Һ����Fe3+����μӷ�Ӧ�����۵�����Ϊ�������������� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2010��ɽ��ʡΫ���и߿���ѧһģ�Ծ��������棩 ���ͣ������
 O2��g���TFeO��s����H=-272kJ?mol-1
O2��g���TFeO��s����H=-272kJ?mol-1
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com