
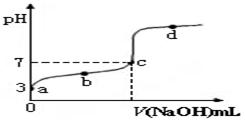
| A.a点时,CH3COOH的电离度是1% |
| B.b点时,溶液中c(CH3COO-)>c(Na+) |
| C.c点表示CH3COOH和NaOH恰好反应完全 |
D.b、d点表示的溶液中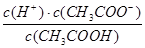 均等于K 均等于K |
科目:高中化学 来源:不详 题型:单选题
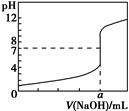
| A.若将盐酸换成同浓度的醋酸溶液,则滴定到pH=7时,a>20.00 |
| B.该滴定也可以用甲基橙作指示剂 |
| C.若用酚酞作指示剂,当滴定到溶液由无色变为红色且半分钟内不褪色时停止滴定 |
| D.滴定过程中,可能存在:c(Cl-)>c(H+)>c(Na+)>c(OH-) |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.利用太阳能等清洁能源代替化石燃料,有利于节约资源、保护环境 |
| B.绿色化学的核心是应用化学原理对环境污染进行治理 |
| C.为防止电池中的重金属等污染土壤和水体,应积极开发废电池的综合利用技术 |
| D.提倡人们购物时不用塑料袋,是为了防止白色污染 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
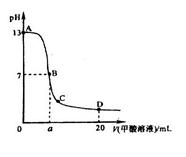
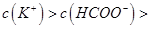
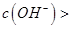
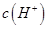
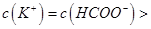
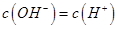 ,且a=7.5
,且a=7.5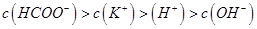
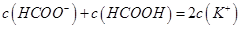
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

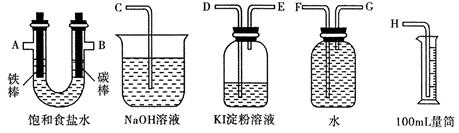
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.移取20 mL待测盐酸溶液注入洁净的锥形瓶中,并加入2~3滴酚酞; |
| B.用标准溶液润洗滴定管2~3次; |
| C.把盛有标准溶液的碱式滴定管固定好,调节滴定管使尖嘴处充满溶液; |
| D.取标准KOH溶液注入碱式滴定管至刻度“0”以上2~3 cm处; |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
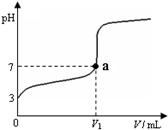
| A.上述 CH3COOH溶液中:c(H+)=1×10-3 mol·L-1 |
| B.图中V1 >20 mL |
| C.a点对应的溶液中:c (CH3COO-)=c (Na+) |
| D.加入NaOH溶液体积为20 mL时,溶液中:c (CH3COOH) + c (H+)=c (OH-)+c(CH3COO-) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com